题目内容
金属活动性顺序在运用中给我们三条判断依据,即在金属活动性顺序里:(1)金属的位置越靠前它的活动性就越强;
(2)位于氢前面的金属能置换出盐酸、稀硫酸中的氢;
(3)位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来.
通过查阅资料我发现金属铝与氧化铜在高温条件下能发生置换反应,其化学方程式为
分析:根据金属活动性顺序的意义进行分析,在金属活动性顺序中,金属的位置越靠前,它的活动性越强,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,利用这些知识结合类比的方法可解决此题.
解答:解:在金属活动性顺序中,金属的位置越靠前,它的活动性越强,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,结合置换反应的规律及有关信息可书写有关的化学方程式,其规律的得出可依据(3)类比书写.
故答案为:2Al+3CuO
3Cu+Al2O3;在高温条件下,位于前面的金属能把位于后面的金属从它们的氧化物里置换出来.
故答案为:2Al+3CuO
| ||
点评:本题考查了金属活动性顺序的意义,完成此题,可以依据已有的知识进行,同时也要求同学们要加强基础知识的储备,以便能灵活应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
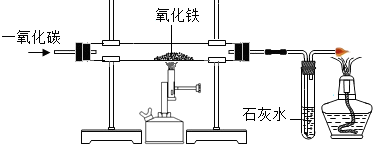 铁、铝、铜是日常生活中使用最广泛的金属.
铁、铝、铜是日常生活中使用最广泛的金属.