��Ŀ����
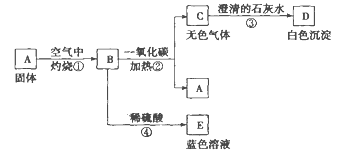
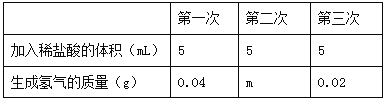
����Ŀ��ij��ȤС�����ô�����������̼������̽����ʵ�鲽�����£�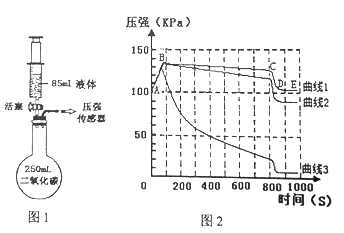
����ͼ1��ʾװ�õ����������ã���ƿ250mL����ƿ���ռ���CO2���壬����ע�����ڸ�װ��85mL��Һ��(�ֱ���ˮ������ʯ��ˮ��40%������������Һ)�����Ӻ�װ�ú�ѹǿ��������
����λͬѧͬʱѸ�ٽ�ע������85mL��Һ��(ˮ������ʯ��ˮ��40%������������Һ)ע�������ƿ�У��رջ�����
��һ��ʱ���ͬʱ����ƿ���۲촫��������ʵʱ�ش�����ƿ����ѹ�仯�γɵ�ͼ�����ͼ2��ʾ���Իش��������⣺
��1����������1��CD����ѹ���ټ�С�IJ����������ı�װ��ҩƷ������£���һ������E��ķ�������
��2������2�з����ķ�Ӧ����ʽΪ������2������3����ϴ��ԭ������
��3���Ա�����1��2��3�����ܵó��Ľ�������
��CO2����ˮ������Ӧ����1���ˮԼ�ܽ�1���CO2����CO2����NaOH��Һ������Ӧ���ܼ���CO2�ñ��ͳ���ʯ��ˮ�Ϻ��ʣ�������CO2��NaOH��Һ�Ϻ���
��4����֪��ʵ�����ṩ������������Һ������Y����ƿ��250mLCO2������������������ɵ�̼��������Ϊ���٣�(��ʵ��������CO2���ܶ�ԼΪ2g/L��������������һλС��)
���𰸡�
��1������ƿ,ʹ��ƿ��������ȴ
��2��CO2+Ca(OH)2=CaCO3��+H2O,����ʯ��ˮŨ��̫��(������������ˮ)Ӱ���˶�����̼������)
��3���٢�
��4���⣺������̼���=250mL=0.25L������̼����=0.25L��2g/L=0.5g��̼���Ƶ�����ΪX,
CO2+2NaOH= | Na2CO3+H2O |
44 | 106 |
0.5g | x |
![]() X= 1.2g������̼�����������Ϊ1.2g ��
X= 1.2g������̼�����������Ϊ1.2g ��
����������1������ƿ�����������������CD����ѹ���ټ�С�����ı�װ��ҩƷ������£���һ������E�㣬����һ������ѹǿ������ʹ��ƿ��������ȴ����2������2�Զ�����̼�����������У�˵��Һ����ʯ��ˮ����Ӧ�Ļ�ѧ����ʽΪ��CO2+Ca(OH)2=CaCO3��+H2O�����ڱ���ʯ��ˮŨ��̫��(������������ˮ)Ӱ���˶�����̼�����գ���������3Ϊ40%������������Һ����3����������1ǰ��ѹǿ�������䣬�ɵ�1���ˮԼ�ܽ�1���CO2����ͬ���ˮ������������Һʱ�Ա�����1��3����������������Һʱ��ѹǿ��С�Ĵ�˵��CO2����NaOH��Һ������Ӧ���Ա�����1��2��3������3ѹǿ�������˵�����ն�����̼��࣬����CO2��NaOH��Һ�Ϻ��ʡ�
���Դ��ǣ�����ƿ��ʹ��ƿ��������ȴ��CO2+Ca(OH)2=CaCO3��+H2O������ʯ��ˮŨ��̫��(������������ˮ)Ӱ���˶�����̼������)���٢ܡ�
�⣺������̼���=250mL=0.25L
������̼����=0.25L��2g/L=0.5g
��̼���Ƶ�����ΪX��
CO2+2NaOH= | Na2CO3+H2O |
44 | 106 |
0.5g | x |
![]()
X= 1.2g
������̼�����������Ϊ1.2g ��
�����㾫�����������⣬������Ҫ�˽������̼�Ļ�ѧ����(��ѧ���ʣ�һ������²���ȼ��,Ҳ��֧��ȼ�գ����ܹ�����������ˮ��Ӧ����̼���ʹ�����ʯ��ˮ����ǣ������ȵ�̼��Ӧ)����Ҫ���ն�����̼����;(��;����𣻼��������������ʣ��������仯ѧ���ʣ��ɱ������˹����ꡢ����������ҷ���)�����֪ʶ���Ǵ���Ĺؼ���