题目内容
【题目】古往今来,金属材料和制品在我们的社会生活中一直起着非常重要的作用。.
(1)写出用CO和磁铁矿为原料炼铁的化学方程式_____。
(2)实验室中用如下实验来研究铁、铝、铜三种金属活动顺序及其在活动顺序表中相对氢的位置.
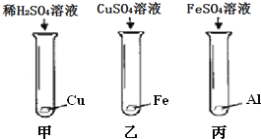
①乙实验观察到的现象是_____。
②若将上述实验之一替换掉一种药品,即可达成实验目的.说明具体的改进方法:_____.
(3)某同学在实验室进行了两个有关金属性质的实验:
实验Ⅰ:硫酸铝溶液和铁粉混合 实验Ⅱ:硫酸铜溶液与铁粉混合
在上述两个实验结束后,该同学将实验Ⅰ和Ⅱ的物质全部倒入同一个烧杯中,发现烧杯内的红色固体明显增多,原因是_____(用文字说明)。一段时间后过滤,向滤渣中滴加盐酸,结果没有气泡产生。那么,滤液中所含金属离子的情况可能是_____(填序号)。
①Al3+ ②Al3+、Fe2+ ③Al3+、Fe3+ ④Fe2+、Cu2+ ⑤Al3+、Fe2+、Cu2+
【答案】4CO+Fe3O4![]() 3Fe+4CO2 铁表面出现红色固体,溶液由蓝色变为浅绿色 将乙实验中的硫酸铜溶液换为稀硫酸 实验Ⅰ中的铁粉与实验Ⅱ中剩余的硫酸铜溶液反应生成硫酸亚铁和铜 ②⑤
3Fe+4CO2 铁表面出现红色固体,溶液由蓝色变为浅绿色 将乙实验中的硫酸铜溶液换为稀硫酸 实验Ⅰ中的铁粉与实验Ⅱ中剩余的硫酸铜溶液反应生成硫酸亚铁和铜 ②⑤
【解析】
(1)磁铁矿的主要成分是四氧化三铁,一氧化碳与四氧化三铁在高温的条件下反应生成铁和二氧化碳,故反应的化学方程式写为:4CO+Fe3O4![]() 3Fe+4CO2。
3Fe+4CO2。
(2)①乙实验是铁与硫酸铜反应生成硫酸亚铁和铜,观察到的现象是铁表面出现红色固体,溶液由蓝色变为浅绿色,故填铁表面出现红色固体,溶液由蓝色变为浅绿色;
②在金属活动性顺序中,铁排在氢的前面,铜排在氢的后面,实验来验证铁、铝、铜三种金属活动顺序及其在活动顺序表中相对氢的位置,可将乙实验中的硫酸铜溶液换为稀硫酸,故填将乙实验中的硫酸铜溶液换为稀硫酸。
(3)实验Ⅰ中硫酸铝溶液和铁粉不能发生反应,实验Ⅰ和Ⅱ的物质全部倒入同一个烧杯中,烧杯内的红色固体明显增多,是实验Ⅰ中的铁粉与实验Ⅱ中剩余的硫酸铜溶液反应生成硫酸亚铁和铜,故填实验Ⅰ中的铁粉与实验Ⅱ中剩余的硫酸铜溶液反应生成硫酸亚铁和铜;
实验Ⅰ中硫酸铝溶液和铁粉不能发生反应,所以滤液中肯定含有硫酸铝,向滤渣中滴加盐酸,结果没有气泡产生,说明铁粉全部参加反应,溶液中肯定有硫酸亚铁,铁粉与硫酸铜反应,铁粉全部参加反应,如果硫酸铜全部参加反应,则滤液中的溶质有硫酸铝和硫酸亚铁,溶液中的阳离子为Al3+、Fe2+,如果硫酸铜部分参加反应,则溶液中的溶质有硫酸铝、硫酸亚铁和硫酸铜,则溶液中的阳离子有Al3+、Fe2+、Cu2+,故填②⑤。

【题目】化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:
(查得资料)
(1)该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体产生。
(2)饱和碳酸氢钠溶液不吸收二氧化碳。
(3)碱石灰的主要成分为氧化钙和氢氧化钠。
(设计实验)小组同学设计了如图所示装置(图中夹持仪器略去)测定牙膏样品中碳酸钙的含量。
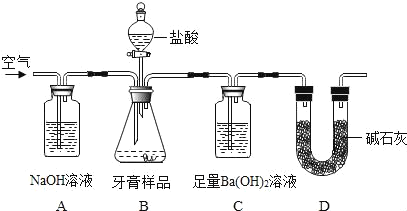
依据图示回答下列问题:
(1)B装置使用分液漏斗的优点是_____。
(2)A中氢氧化钠溶液的作用是_____。
(3)C中观察到有沉淀产生,反应的化学方程式为_____。
(4)实验过程中需持续缓缓通入空气,其作用有_____。
(解释与结论)将C中产生沉淀通过_____、洗涤、干燥、称量,通过计算求得牙膏样品中碳酸钙的含量。
(反思与评价)
反思实验过程,小刚同学提出应采取必要措施,提高测定准确度。他提出的下列各项措施中,不能提高测定准确度的是_____(填字母序号)。
a 在加入盐酸之前,排净装置内的CO2气体
b 放慢滴加盐酸的速度
c 在A﹣B之间增添盛有浓硫酸的洗气装置
d 在B﹣C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(拓展延伸)小亮同学为确定A中溶质成分,进行了如表所示实验:
实验操作 | 实验现象 | 实验结论 |
(1)、取少量滤液于试管中,加入足量____ | 产生白色沉淀 | 溶质主要成分为Na2CO3和NaOH |
(2)、过滤,取少量滤液加入 | _____ |
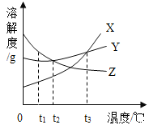
【题目】依据下列实验和数据回答以下小题。KCl和KNO3的溶解度曲线如下图所示。
| 序号 | ① | ② | ③ | ④ |
固体种类 | KNO3 | KCl | KCl | KCl | |
固体的质量/g | 25 | 25 | 25 | 50 | |
温度/oC | 10 | 10 | 30 | 50 |

【1】①~④所得溶液属于饱和溶液的是
A. ①③B. ①④C. ②③D. ②④
【2】下列关于①~④所得溶液的说法不正确的是
A. 溶质质量:① < ②B. 溶液质量: ③ < ④
C. 溶质质量分数:② = ③D. ④中溶质与溶剂的质量比为1:2
【题目】某小组对“化学红绿灯”实验感兴趣,进行以下实验,探究温度和靛蓝胭脂红溶液浓度对变色所需时间的影响。
(查阅资料)靛蓝胭脂红是一种指示剂;向靛蓝胭脂红和氢氧化钠的混合液(绿色)中,加入葡萄糖,静置时靛蓝胭脂红与葡萄糖逐步反应,而产物在振荡时又能与空气中的氧气反应,再逐步转化成靛蓝胭脂红。颜色变化可循环多次,过程如下:
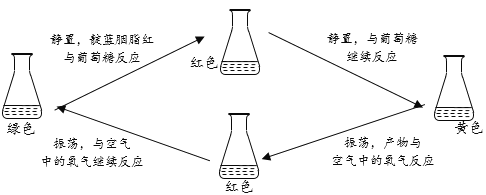
(进行实验)
在锥形瓶中分别加入表中试剂,充分混合后,溶液为绿色。静置,观察并记录。
实验序号 | 0.1%靛蓝胭脂红溶液体积 / mL | 2%氢氧化钠溶液体积/ mL | 18%葡萄糖溶液体积 / mL | 水体积 / mL | 温度/℃ | 变色时间/s | |||
绿→红 | 红→黄 | 合计 | |||||||
① | 10 | 70 | 10 | 10 | 20 | 178 | 81 | 259 | |
② | 10 | 70 | 10 | 10 | 40 | 22 | 21 | 43 | |
③ | 10 | 70 | 10 | 10 | 60 | 6 | 5 | 11 | |
④ | 20 | 70 | 10 | 0 | 40 | 21 | 27 | 48 | |
⑤ | 5 | 70 | 10 | x | 40 | 25 | 5 | 30 | |
注:所用溶液的密度均按1 g/mL计。
(解释与结论)
(1)靛蓝胭脂红的化学式为C16H8N2Na2O8S2,碳元素与氢元素的质量比是______。
(2)实验⑤中,x =______mL。
(3)实验①②③的结论是______。
(4)能证明靛蓝胭脂红溶液浓度对变色所需时间有影响的实验是______(填序号)。
(反思与评价)
(5)上述实验循环多次后,当葡萄糖完全反应后,再经充分振荡、静置后,溶液颜色最终为______。
(6)除上述实验探究的因素外,还可能有的影响因素是______(写出一条即可)。
【题目】下表提供的四组物质符合图示相连物质间在一定条件下可以发生反应的是
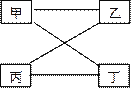
甲 | 乙 | 丙 | 丁 | |
A | CO | O2 | H2SO4 | CuO |
B | Mg | HCl | CuSO4 | NaOH |
C | KOH | SO3 | NaOH | CuSO4 |
D | Na2CO3 | Ca(OH)2 | HCl | CaCl2 |