题目内容
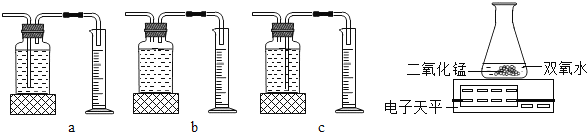
【题目】小明同学配制100g 10%的氯化钠溶液,整个操作过程如下图所示:回答下列问题:
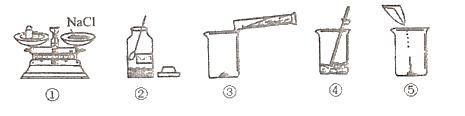
(1)图②中盛放氯化钠的固体的仪器名称是______,其中操作错误的是_______(填序号)
(2)配制溶液的正确操作顺序为__________ (填序号)
(3)量水时选用的量筒的量程最合适的是_________,(填序号)
A.10 ml B.25 ml C.50m D.100ml
(4)经检测,该同学配制的溶液溶质质量分数偏小,可能的原因是______ (填序号)
A.氢氧化钠固体不纯 B.用生锈的砝码称量
C.装瓶时有少量溶液洒出 D.溶解时烧杯内壁有水珠
(5)请你帮小明完成以下计算:
①要配制100g 10%的氯化钠的溶液,需要称取食盐____ g, 加入水_____ g。
②若要将100g 10%的氯化钠溶液稀释成2%,需要加入水的质量_______g。
【答案】广口瓶 ① ②①⑤③④ D AD 10 90 400
【解析】
(1)图②中盛放氯化钠的固体的仪器名称是广口瓶,其中操作错误的是操作①,没有遵循左物右码的原则;
(2)配制溶液的正确操作顺序为计算、称量、溶解、装瓶存放,所以为②①⑤③④;
(3)根据一次性量完并且与被量液体体积相近的原则,该实验中量水时选用的量筒的量程最合适的是100ml的量筒;
(4)配制的溶液溶质质量分数偏小的原因是溶质的质量少了或溶剂的量多了。
A.氢氧化钠固体不纯,导致溶质偏少,溶液溶质质量分数会偏小; B.生锈的砝码质量比原砝码增加,用生锈的砝码称量,导致称量到的氢氧化钠质量增加,溶液溶质质量分数会偏大;C.溶液是均一、稳定的,装瓶时有少量溶液洒出,溶液的质量会减少,但是溶质的质量分数不变; D.溶解时烧杯内壁有水珠,溶剂的量偏多,溶质的质量分数偏小。故选AD;
(5)①要配制100g 10%的氯化钠的溶液,需要称取食盐100g ×10%g=10g,加入水100g-10g=90 g;
②设要将100g 10%的氯化钠溶液稀释成2%,需要加入水的质量为x,
100g× 10%=(100g+x)2% x=400g。