题目内容
【题目】同学们总结归纳了二氧化碳的实验室制法,并利用下列装置进行练习和拓展。

(一)、知识总结:
【实验仪器】写出装置图中标号仪器的名称:a____________
【反应原理】用大理石与稀盐酸制取二氧化碳的化学方程式为______________。
【气体制备】
①用不同的药品制取气体,发生装置可能不同。确定发生装置时应考虑的因素是______________。
A. 反应是否需要加热 B. 反应物的密度
C. 反应物是固体还是液体 D. 反应物的纯度
②用大理石与稀盐酸制取二氧化碳,装置C较装置B的优点是_________________。
③装置B和装置C中的长颈漏斗______________(填编号字母) 改成分液漏斗。
A.都能 B.都不能 C. 装置B能,装置C不能 D.装置B不能,装置C能
【气体收集】实验室收集CO2的装置是______________(填装置图序号)。
【气体验满】检验CO2是否收集满的方法是 _____________________。
(二)、知识拓展:请仔细观察下列装置图的特点并回答相关问题:
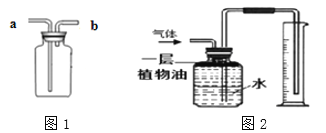
实验室若用图1装置收集CO2,则CO2应从___________口进入(填“a”或“b”)
② 用图2装置可收集一定体积的CO2,植物油的作用是_______________。
【答案】 锥形瓶 CaCO3+2HCl→CaCl2+H2O+CO2↑ A、C(全对得1分) C装置能随时控制反应的发生和停止 C E 点燃的木条放在瓶口熄灭 a 防止二氧化碳溶于水(和与水反应)

 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案【题目】一包干燥的红色粉末是Cu、Fe2O3的混合物,同学们为确定红色粉末的组成比例,称取该粉末5.0g装硬质玻璃管中,按右下图在通风橱中进行实验。开始时缓缓通入CO气体,过一段时间后再加热使其充分反应。待反应完全后,停止加热,继续通CO气体直至玻璃管冷却。
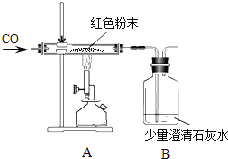
在装置A中先通CO气体的目的是_____________
②反应前后称量相关装置和物质的总质量,其数据如下表:
反应前 | 反应后 |
玻璃管和红色粉末的总质量为37.3g | 玻璃管和固体物质的总质量为36.1g |
小组内小丁同学分析表中的数据后,得出红色粉末中氧元素的质量为___________。
A装置中发生反应的化学方程式__________
③小组内小林同学认为为了防止溶液倒吸,本实验停止加热前应先断开A和B的连接,你认为是否需要?为什么?___________
④实验后小组内有同学指出:上述装置未进行尾气的处理。于是有同学设计了用下图装置代替原装置,实验装置图中采用虚线框内的装置,其作用是____________
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳

【题目】实验室常用下列装置来制取气体,并完成相关性质实验探究。回答有关问题:
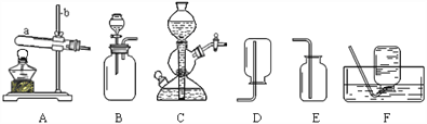
① 仪器a、b的名称是____________、 __________。
② 实验室用氯酸钾和二氧化锰混合共热制取一瓶干燥的氧气,需要选择的装置组合
是_________,化学方程式是____________。
③ 实验室用块状大理石和稀盐酸反应制取二氧化碳气体,选择的发生装置是C,该发生装置的名称叫___________,优点是__________,图示为反应的_____(填“进行”或“停止”)状态;充分反应后,向反应后的混合溶液中加入锌粒,产生气泡,则混合溶液中的溶质成分为________(填写化学式)。
④ 同学们在进行实验探究时发现很多因素都会对实验结果产生影响。
实验 | 分析与结论 |
Ⅰ.硫在空气中燃烧发出微弱的淡蓝色火焰, 硫在氧气中燃烧发出______________。 | 说明反应物的浓度不同,反应现象不同。 |
Ⅱ.细铁丝在氧气中易燃烧,化学方程式是________, 粗铁丝在氧气中不易燃烧。 | 说明_____________, 反应的速率不同。 |
Ⅲ.碳在氧气不足的条件下燃烧生成一氧化碳, 碳在氧气充足的条件下燃烧生成二氧化碳。 | 说明反应物的用量不同,________。 |