题目内容
【题目】已知:Cu2O+H2SO4=Cu+CuSO4+H2O将14.4gCu2O、Cu混合物溶于100.0g溶质质量分数为9.8%的稀H2SO4中,搅拌使之充分反应,过滤、洗涤、干燥得10.4g固体。下列说法正确的是()
A.10.4g固体是反应生成的铜的质量
B.反应后溶液呈蓝色,溶液中只含有CuSO4,不含H2SO4
C.原混合物中Cu2O与Cu的质量之比为1:1
D.反应后溶液中CuSO4的溶质质量分数为8.0%
【答案】C
【解析】
设参加反应的氧化亚铜的质量、消耗的硫酸的质量以及生成的铜的质量和硫酸铜的质量分别为x、y、z、w
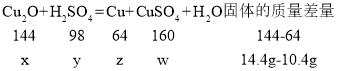
![]() 解得x=7.2g、y=4.9g、z=3.2g、w=8g
解得x=7.2g、y=4.9g、z=3.2g、w=8g
而稀硫酸中的硫酸的质量为100.0g×9.8%=9.8g,所以硫酸有剩余,即氧化亚铜完全反应。
A、10.4g 固体不完全是反应生成的铜的质量,是生成的铜和原混合物中的铜的质量,故错误;
B、反应后溶液呈蓝色,溶质是生成硫酸铜和剩余的稀硫酸,所以应该为两种。错误;
C、原混合物中 Cu2O 与Cu的质量之比为7.2g:(14.4g-7.2g)=1:1,正确;
D、反应后溶液中 CuSO4的溶质质量分数为为![]() ×100%≈7.8%.而非8%.错误。故选:C。
×100%≈7.8%.而非8%.错误。故选:C。

 出彩同步大试卷系列答案
出彩同步大试卷系列答案【题目】某学生用下图的实验装置进行实验。
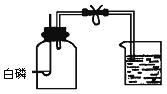
实验步骤 | 简 答 |
①先用夹子夹紧橡皮管 | |
②将燃烧匙插入广口瓶 | 使瓶塞与广口瓶塞紧,防止_______。 |
③用聚光灯照射点燃燃烧匙内的白磷 | 白磷燃烧的现象:_______。白磷燃烧的文字表达式:_____。 |
④燃烧完毕,打开夹子 | 水倒流入A瓶且明显少于广口瓶容积的1/5。 |
问题探究:
(1)请你归纳,该实验的目的:_____;
(2)请你分析后提出,可能造成实验值偏小的原因①_____;②_____;
【题目】对下列实验指定容器中的水,其解释没有体现水的主要作用的是![]()
![]()
A | B | C | D | |
实 验 装 置 |
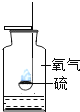
硫在氧气中燃烧 |
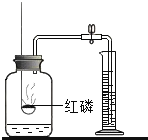
测定空气中氧气含量 |
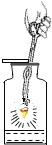
铁丝在氧气中燃烧 |
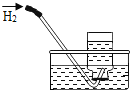
排水法收集氢气 |
解释 | 集气瓶中的水: 吸收有害气体 | 量筒中的水: 通过水体积的变化得出 | 集气瓶中的水: 吸收溅落融熔物 | 集气瓶中的水: 水先将集气瓶内的空气排净,后便于观察 |
A. A B. B C. C D. D
【题目】某化学兴趣小组进行化学课外活动,实验室提供以下药品:肥皂水、澄清石灰水、铁粉、二氧化锰、活性炭。请你与他们完成下列实验报告。
实验目的 | 实验操作 | 预期现象与结论 |
1、探究薯片包装袋的气体,该气体可能是氮气、二氧化碳 | 用注射器抽取薯片包装袋中的气体,把气体通入剩有适量_______________的试管中,观察现象 | _________________,说明该气体不是二氧化碳。 |
2、鉴别过氧化氢溶液、和蒸馏水两瓶液体。 | 分别取少量液体于两支试管中,向其中加入适量的____________,观察现象。 | 试管内__________________, 说明该原液体为过氧化氢溶液,不是蒸馏水。反应的文字表达式为____________ |