题目内容
 (2012?龙岩)胃酸过多须服用抗酸药物(能与盐酸反应).如图为铝碳酸镁说明书的部分内容.兴趣小组对该药物开展如下探究.
(2012?龙岩)胃酸过多须服用抗酸药物(能与盐酸反应).如图为铝碳酸镁说明书的部分内容.兴趣小组对该药物开展如下探究.I.该药物抗酸作用的探究
资料表明,铝碳酸镁[其主要成分的化学式为AlMg(OH)3CO3]与盐酸反应的化学方程式为:AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑
(1)将反应产生的气体通入澄清石灰水,将观察到的现象是
澄清石灰水变浑浊
澄清石灰水变浑浊
,该反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O
Ca(OH)2+CO2=CaCO3↓+H2O
.(2)该物质中含有Al3+、Mg2+、OH-和CO32-.结合该物质与盐酸反应的化学方程式分析,该药物起抗酸作用(降低胃液酸性)的微粒是
OH-
OH-
、CO32-
CO32-
(填微粒符号).II.服用方法的探究
该抗酸药为什么要求“嚼碎后服用”?小红猜想可能是“对于相同质量的药片,嚼碎后服用,将消耗更多的胃酸”,小明则认为“嚼碎后药物将与胃液中的盐酸反应快”.
(3)显然,小红猜想是错误的.原因是
嚼碎后药片质量没有增加
嚼碎后药片质量没有增加
.(4)小明设计了如下实验来证明自己的猜想:
【实验1】将一片完整的药片放入试管中,向其中加入5mL 5%的稀盐酸;
【实验2】将一片完整的药片研碎后放入试管中,向其中加入5mL 5%的稀盐酸.
对比实验1和实验2,小明观察到的现象为
实验2比实验1反应更快
实验2比实验1反应更快
,证明了他的猜想正确.III.主要成分含量的探究
(5)兴趣小组取6片药片粉碎后放入试管中,向其加入足量的稀盐酸,充分反应后放出气体0.88g.试通过计算,每片药物中含有AlMg(OH)3CO3的质量是多少?(结果保留到0.1)
(已知:药物所含其他成分不与稀盐酸反应;AlMg(OH)3CO3的相对分子质量为162)
分析:(1)根据二氧化碳能使澄清石灰水变浑浊进行解答;
(2)根据氢氧化根离子和碳酸根离子和酸中的氢离子反应进行解答;
(3)根据嚼碎后药片质量没有增加进行解答;
(4)根据实验2比实验1反应更快可以证明小明的猜想正确进行解答;
(5)根据二氧化碳的质量求出AlMg(OH)3CO3的总质量进而求出每片药物中含有AlMg(OH)3CO3的质量进行解答.
(2)根据氢氧化根离子和碳酸根离子和酸中的氢离子反应进行解答;
(3)根据嚼碎后药片质量没有增加进行解答;
(4)根据实验2比实验1反应更快可以证明小明的猜想正确进行解答;
(5)根据二氧化碳的质量求出AlMg(OH)3CO3的总质量进而求出每片药物中含有AlMg(OH)3CO3的质量进行解答.
解答:解:(1)二氧化碳能使澄清石灰水变浑浊生成碳酸钙和水,反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O;
(2)氢氧化根离子和酸中的氢离子反应生成水,碳酸根离子和酸中的氢离子反应生成水和二氧化碳,而铝离子和镁离子不和酸中的氢离子反应,该药物起抗酸作用(降低胃液酸性)的微粒是OH-和CO32-;
(3)嚼碎后药片质量没有增加,所以嚼碎后服用,不会消耗更多的胃酸;
(4)实验2比实验1反应更快可以证明小明的猜想正确;
(5)解:6片药物中含AlMg(OH)3CO3的质量为x
AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑
162 44
x 0.88g
=
解得:x=3.24 g
每片药物中含AlMg(OH)3CO3的质量=3.24 g÷6=0.5g
答:每片药物中含AlMg(OH)3CO3的质量为0.5 g.
故答案为:(1)澄清石灰水变浑浊;Ca(OH)2+CO2=CaCO3↓+H2O;
(2)OH-和;CO32-;
(3)嚼碎后药片质量没有增加;
(4)实验2比实验1反应更快;
(5)0.5 g.
(2)氢氧化根离子和酸中的氢离子反应生成水,碳酸根离子和酸中的氢离子反应生成水和二氧化碳,而铝离子和镁离子不和酸中的氢离子反应,该药物起抗酸作用(降低胃液酸性)的微粒是OH-和CO32-;
(3)嚼碎后药片质量没有增加,所以嚼碎后服用,不会消耗更多的胃酸;
(4)实验2比实验1反应更快可以证明小明的猜想正确;
(5)解:6片药物中含AlMg(OH)3CO3的质量为x
AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑
162 44
x 0.88g
| 162 |
| x |
| 44 |
| 0.88g |
解得:x=3.24 g
每片药物中含AlMg(OH)3CO3的质量=3.24 g÷6=0.5g
答:每片药物中含AlMg(OH)3CO3的质量为0.5 g.
故答案为:(1)澄清石灰水变浑浊;Ca(OH)2+CO2=CaCO3↓+H2O;
(2)OH-和;CO32-;
(3)嚼碎后药片质量没有增加;
(4)实验2比实验1反应更快;
(5)0.5 g.
点评:化学反应的实质是分子的破裂和原子的重新组合,这个过程中浓度越高或者说反应物之间的接触面积越大,反应进行也就越快.所以反应速率的改变就要从接触面积的角度去思考.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目
(2009?龙岩)碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.
实验一:探究碳酸氢钠溶液的酸碱性
用pH试纸测得碳酸氢钠溶液的pH为10,由此可知碳酸氢钠溶液呈性.
实验二:探究碳酸氢钠的热稳定性
[查阅资料]碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种常见的固体物质.
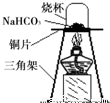
[进行实验]为验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的 碳酸氢钠到铜片上加热,如右图所示.
(1)加热一段时间后,观察到烧杯内壁有.
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊.写出该反应的化学方程式.
(3)兴趣小组的同学认为充分加热后的固体产物可能是NaOH或Na2CO3.
①他们猜想的依据是.
②请设计实验检验反应后的固体产物是NaOH还是Na2CO3,并填入下表(只要求填写其中一行.若两行都写,按第一行计分):
[拓展应用]碳酸氢钠、碳酸钙、氢氧化镁等常用于制作抗酸药,用来治疗胃酸过多.但对于
患有胃溃疡(胃黏膜溃烂)的病人在胃酸过多时,却不宜服用碳酸氢钠、碳酸钙等碳酸盐,
其原因是.
实验一:探究碳酸氢钠溶液的酸碱性
用pH试纸测得碳酸氢钠溶液的pH为10,由此可知碳酸氢钠溶液呈性.
实验二:探究碳酸氢钠的热稳定性
[查阅资料]碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种常见的固体物质.
[进行实验]为验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的 碳酸氢钠到铜片上加热,如右图所示.
(1)加热一段时间后,观察到烧杯内壁有.
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊.写出该反应的化学方程式.
(3)兴趣小组的同学认为充分加热后的固体产物可能是NaOH或Na2CO3.
①他们猜想的依据是.
②请设计实验检验反应后的固体产物是NaOH还是Na2CO3,并填入下表(只要求填写其中一行.若两行都写,按第一行计分):
| 实验操作 | 预期现象 | 结论 |
| 固体产物是Na2CO3,而不是NaOH | ||
| 固体是产物NaOH,而不是Na2CO3 |
患有胃溃疡(胃黏膜溃烂)的病人在胃酸过多时,却不宜服用碳酸氢钠、碳酸钙等碳酸盐,
其原因是.

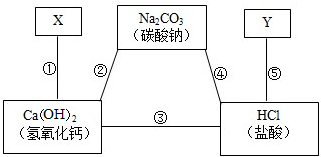 (2012?荆州)李红同学在复习元素化合物知识时,归纳了如图所示的物质间关系.图中横线两端的物质在一定条件下都能发生化学反应;X、Y是初中化学中常见的一种单质和一种化合物,且此化合物与图中已知物的类型不同.请你回答:
(2012?荆州)李红同学在复习元素化合物知识时,归纳了如图所示的物质间关系.图中横线两端的物质在一定条件下都能发生化学反应;X、Y是初中化学中常见的一种单质和一种化合物,且此化合物与图中已知物的类型不同.请你回答: