题目内容
某班同学要测定实验室中氯酸钾的纯度(药品中含氯酸钾的质量分数).甲、乙两组同学分别取10g氯酸钾样品和5g二氧化锰混合均匀,加热使其充分反应.甲组同学测定产生的氧气体积为2.74L(密度为1.40g/L),乙组同学称量反应后固体物质质量为11.16g.
(1)请你利用甲组同学的数据计算氯酸钾的纯度.(计算结果精确到0.1g)
(2)乙组同学通过计算也得到了氯酸钾的纯度,请利用乙组同学的数据再计算一次.
解:(1)甲组同学产生的氧气的质量为:1.40g/L×2.74L=3.836g
设氯酸钾样品中氯酸钾的质量为x,
2KClO3 2KCl+3O2↑
2KCl+3O2↑
245 96
x 3.836g
 x=9.8g
x=9.8g
 =98%
=98%
(2)根据质量守恒定律,乙组同学产生氧气的质量为:10g+5g-11.16g=3.84g.
设氯酸钾样品中氯酸钾的质量为y,
2KClO3 2KCl+3O2↑
2KCl+3O2↑
245 96
x 3.84g
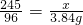 x=9.8g
x=9.8g
 =98%
=98%
答:(1)甲组同学的数据计算氯酸钾的纯度为98%;(2)乙甲组同学的数据计算氯酸钾的纯度为98%.
分析:(1)由产生氧气的体积、密度,根据反应的化学方程式计算出原混合物中氯酸钾的质量,进而计算出氯酸钾的纯度即可.
(2)根据质量守恒定律,反应前后固体混合物减少的质量为氧气的质量,根据反应的化学方程式计算出原混合物中氯酸钾的质量,进而计算出氯酸钾的纯度即可.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出氧气的质量是乙组正确解答本题的前提和关键.
设氯酸钾样品中氯酸钾的质量为x,
2KClO3
 2KCl+3O2↑
2KCl+3O2↑245 96
x 3.836g
 x=9.8g
x=9.8g =98%
=98%(2)根据质量守恒定律,乙组同学产生氧气的质量为:10g+5g-11.16g=3.84g.
设氯酸钾样品中氯酸钾的质量为y,
2KClO3
 2KCl+3O2↑
2KCl+3O2↑245 96
x 3.84g
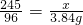 x=9.8g
x=9.8g =98%
=98%答:(1)甲组同学的数据计算氯酸钾的纯度为98%;(2)乙甲组同学的数据计算氯酸钾的纯度为98%.
分析:(1)由产生氧气的体积、密度,根据反应的化学方程式计算出原混合物中氯酸钾的质量,进而计算出氯酸钾的纯度即可.
(2)根据质量守恒定律,反应前后固体混合物减少的质量为氧气的质量,根据反应的化学方程式计算出原混合物中氯酸钾的质量,进而计算出氯酸钾的纯度即可.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出氧气的质量是乙组正确解答本题的前提和关键.

练习册系列答案
相关题目