题目内容
家里蒸馒头用的纯碱中常含有少量的氯化钠,某实验小组要测完该纯碱中碳酸钠的含量,现取该纯碱样品8g,加入一定质量的某稀盐酸中到不再产生气泡为止,得到2.2g气体,试计算并回答
(1)纯碱样品中碳酸钠的质量分数?
(2)反应后所得氯化钠溶液中溶质的质量?
(3)你能否算出反应后所得到溶液中溶质质量分数 ,你的理由是 .
(1)66.25%;(2)8.55g;(3)不能;不能计算反应后溶液的质量.
解析试题分析:(1)设纯碱样品中碳酸钠的质量为x,同时生成氯化钠的质量为y
Na2CO3+2HCl═2NaCl+CO2↑+H2O
106 117 44
x y 2.2g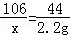

解得:x=5.3g y=5.85g
纯碱样品中Na2CO3的质量分数为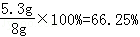
(2)反应后所得氯化钠溶液中溶质的质量为:5.85g+8g﹣5.3g=8.55g
答:(1)纯碱样品中碳酸钠的质量分数为66.25%;
(2)反应后所得氯化钠溶液中溶质的质量为8.55g.
(3)根据溶液中溶质的质量分数的计算公式可以知道,若求算反应后溶液中溶质的质量分数,必须知道反应后溶液的质量和反应后溶质的质量,而本题中不知道加入的盐酸的质量,所以不能计算反应后溶液的质量,故反应后溶液中溶质的质量分数也就无从求算.
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
⑴一定条件下,下列物质在密闭容器内充分反应,反应前后各物质的质量如下:
| 物质 | A | B | C | D |
| 反应前的质量/g | 1.7 | 2.2 | 7.9 | 0.9 |
| 反应后的质量/g | 待测 | 6.6 | 0 | 2.7 |
则:①反应后A的待测质量为 ; ②该反应所属的基本反应类型是 ;
③反应中B和D两种物质变化的质量比为 (最简整数比)。
⑵人体缺少钙元素会影响健康,因此每日需摄人足够的钙。目前市场上的补钙药剂很多,以下是某品牌补钙药剂说明书的部分信息。请仔细阅读后进行计算:

①葡萄糖酸钙的相对分子质量为____________。
②葡萄糖酸钙中碳、氢、氧、钙四种元素的质量比为 。
③(葡萄糖酸钙中钙元素的质量分数为多少?(保留至0.1%,写计算过程,下同)
④按照说明书的用量,每天可补充多少mg钙元素?(精确到0.1)
 3Fe+4CO2.用100t含Fe3O480%的磁铁矿石,理论上冶炼含杂质4%的生铁多少?(答案保留一位小数)
3Fe+4CO2.用100t含Fe3O480%的磁铁矿石,理论上冶炼含杂质4%的生铁多少?(答案保留一位小数)