题目内容
【题目】元素周期表是学习和研究化学的重要工具,下表是元素周期表的部分内容,请认真分析并回答下列问题:

(1)请从上表中查出铝元素的相对原子质量为______;
(2)不同种元素最本质的区别是______![]() 填序号
填序号![]() ;
;
A相对原子质量不同 B质子数不同 C中子数不同
(3)金属Na、Mg化学性质不同的原因是______;
(4)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,请写出其中一条:______。
【答案】26.98 B 最外层电子数不相等 电子层数相等(合理即可)
【解析】
元素周期表中,方格中左上角是原子序数,右上角是元素符号,中间是元素名称,下面是相对原子质量;
一般情况下,最外层电子数小于4的,反应中容易失去电子,大于4的反应中容易得到电子,等于4的,既不容易得到电子,也不容易失去电子,因此最外层电子数相等的元素化学性质相似,最外层电子数是8的是一种稳定结构,第一层也是最外层时,达到2个电子也是一种稳定结构。
(1)铝元素的相对原子质量为26.98。故填:26.98。
(2)元素是具有相同质子数的一类原子的总称;不同种元素最本质的区别是质子数不同。故填:B。
(3)元素的化学性质与原子最外层电子数关系密切。金属Na、Mg化学性质不同的原因是最外层电子数不相等。
故填:最外层电子数不相等。
(4)同一周期元素之间的排列有一定的规律,例如电子层数相等,最外层电子数依次递增等。
故填:电子层数相等(合理即可)。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某气体X可能是由H2、CO、CO2中的一种或两种组成,为了解其组成情况,某同学设计了如下装置进行实验,(假设各步反应均完全,NaOH溶液用于吸收CO2)。

(1)请根据下表中对可能出现的实验现象的描述,推测气体X的组成情况,
可能出现的实验现象 | 气体X的组成 | |||
A中液体 | B中黑色粉末 | C中液体 | ||
① | 不浑浊 | 变成亮红色 | 不浑浊 | _____ |
② | 不浑浊 | 变成亮红色 | 变浑浊 | _____ |
③ | 变浑浊 | 变成亮红色 | 不浑浊 | _____ |
④ | 变浑浊 | 变成亮红色 | 变浑浊 | _____ |
(2)装置中氢氧化钠溶液的作用是_____。
【题目】制作糕点常用Na2CO3或NaHCO3做膨松剂,同学们根据Na2CO3和NaHCO3的性质进行了一系列探究。
(1)NaHCO3和Na2CO3性质差异的探究
[查阅资料]
物质 | Na2CO3 | NaHCO3 | |||||
酸碱性 | 水溶液显碱性 | 水溶液显弱碱性 | |||||
热稳定性 | 受热不分解 | 270℃时完全分解 | |||||
溶解度 | 10℃ | 20℃ | 30℃ | 40℃ | |||
Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g | |||
NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g | |||
(实验探究)
①验证水溶液的酸碱性的差异:分别测两种物质溶液的pH值,请写出测定pH值的方法____________,测定结果:NaHCO3的pH值___________Na2CO3(填“>”或”“<”)。
②验证两种粉末的稳定性:观察到装置中__________(填“甲”或“乙”)烧杯中澄清石灰水变浑浊,该烧杯中发生的反应方程式为_______________。

③利用溶解度的差异鉴别NaHCO3和Na2CO3:小方同学分别取Xg两种固体粉末加入20℃,10g水中充分溶解,通过观察现象区分出碳酸钠和碳酸氢钠,X可以是下列的___________。
A2g B0.96g C0.5g D3g
(2)测定某NaHCO3和Na2CO3混合物中NaHCO3的质量分数利用如图装置进行实验,装置B中放有10g该样品(整套装置气密性良好,各装置中气体吸收剂足量)。
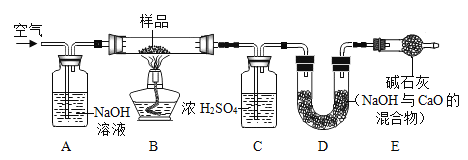
①实验前测定装置D的质量为122.2g,上图装置C的作用是_______________,装置E的作用是_____________,若没有装置E,造成测定结果____________(填“偏大”、“不变”或“偏小”)。
②实验过程中必须向装置内通入空气,装置A中发生的化学反应方程式______________,若没有装置A,造成测定结果_______(填“偏大”、“不变”或“偏小”)。在加热前,先对装置A、B和C(已连接)通一段时间的空气,再连接上装置D、E,目的是_______________;在停止加热后,仍继续通入空气一段时间,目的是____________________。