题目内容
【题目】某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出。这一现象激发起同学们的探究欲望,生成的是什么气体?
【提出猜想】从物质组成元素的角度,放出的气体可能是SO2、O2、H2中的一种或几种。
【查阅资料】SO2易溶于水,它能与NaOH反应,生成Na2SO3和H2O。
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O2,若要检验可以用 ;
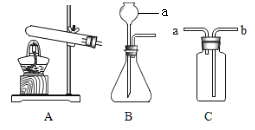
(2)乙同学认为是SO2,则只需将放出的气体通入盛有NaOH溶液的洗气瓶中,称量通气前后洗气瓶的质量。写出SO2与NaOH反应的化学方程式 ;

(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体。如果放出的气体是H2,在B中玻璃管内可观察到的现象是 ,引起该现象的反应方程式为 ;丙同学认为:为确保安全,实验前应先 ,方可采用上面的装置进行实验。
【答案】(1)带火星的木条
(2)2NaOH+SO2=Na2SO3+H2O
(3)黑色铜网变红,有水珠出现;
H2+CuO![]() Cu+H2O(4)验纯
Cu+H2O(4)验纯
【解析】
试题分析:认为是O2,若要检验可以用带火星的木条;乙同学认为是SO2,则只需将放出的气体通入盛有NaOH溶液的洗气瓶中,称量通气前后洗气瓶的质量。SO2与NaOH反应的化学方程式2NaOH+SO2=Na2SO3+H2O;如果放出的气体是H2,在B中玻璃管内可观察到的现象是黑色铜网变红,有水珠出现;因为氢气会和氧化铜反应得到铜和水,引起该现象的反应方程式为H2+CuO![]() Cu+H2O;为确保安全,实验前应先验纯,方可采用上面的装置进行实验,因为氢气具有可燃性,防止爆炸发生。
Cu+H2O;为确保安全,实验前应先验纯,方可采用上面的装置进行实验,因为氢气具有可燃性,防止爆炸发生。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目