��Ŀ����
����Ŀ��ijУ���꼶�����ǰ���ѧ���С���ͬѧ��̽���˹�������(Na2O2)���������(SO2)��Ӧ�����ù������ijɷ֣��������£�
���������ϡ������������������Ӧ�Ļ�ѧ����ʽΪ��2SO2+2Na2O2=2Na2SO3+O2��2Na2SO3+O2= 2Na2SO4��SO2��ʹƷ����Һ��ɫ��
��������롿����1������ɷ�ΪNa2SO3
����2������ɷ�ΪNa2SO4
����3������ɷ�Ϊ_________________
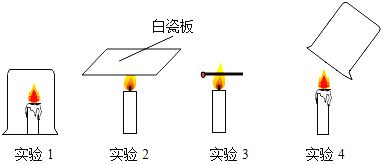
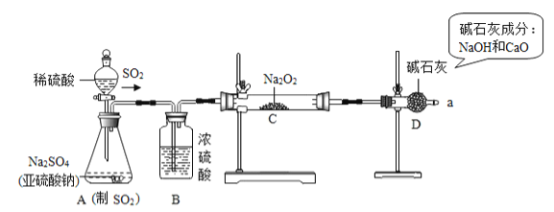
��ʵ��̽��������ͼ��ʾ��װ�ý���ʵ�飮��A�з�Һ©���Ļ�������Ӧ����(����������SO2)���ô����ǵ�ľ�������a�����������壬ľ����ȼ��ʵ��ǰ�Ƶ�Na2O2���������Ϊ78g����ַ�Ӧ��Ƶ���������������Ϊ134g��
��ʵ����ۡ�
(1)A����ȡSO2�����װ�ã���Ӧ�Ļ�ѧ����ʽ��ʵ������ȡCO2�Ļ�ѧ����ʽ���ƣ���д��A�з�����Ӧ�Ļ�ѧ����ʽ��____________________________��
(2)������_________________________________________��ʵ�������Ʋ����2�Ǵ���ģ�
(3)װ��B��������_____________��װ��D��������_____________________________��
(4)���ݷ�Ӧǰ�������������ɼ����Na2SO3������Ϊ______g��Na2SO4������Ϊ______g��
���ܽ�������
(1)��ʵ��ǰ�Ƶ�Na2O2���������Ϊm1g����ַ�Ӧ��Ƶ��������������Ϊm2g����m2��ȡֵ��Χ��_____________________(�ú�m1�Ĺ�ϵʽ��ʾ)��
(2)���������һ��ʵ�鷽����������֤�����������������Ӧ�����ù������ijɷ֣�_________��
���𰸡� Na2SO3��Na2SO4 Na2SO3+H2SO4=Na2SO4+H2O+SO2�� �ô����ǵ�ľ�������a�����������壬ľ����ȼ ����SO2 ��ֹ�������������ŷ��ڻ����кͷ�ֹ�����еĶ�����̼��ˮ��������C�� 126 8 ![]() g��m2��
g��m2��![]() m1g ����ɫ��������ˮ���μ����ᣬ�ռ����壬������ͨ��Ʒ����Һ����Ʒ����ɫ����˵������Na2SO3������Ϊ������
m1g ����ɫ��������ˮ���μ����ᣬ�ռ����壬������ͨ��Ʒ����Һ����Ʒ����ɫ����˵������Na2SO3������Ϊ������
����������������롿�����������������Ӧ�Ļ�ѧ����ʽΪ��2SO2+2Na2O2=2Na2SO3+O2��2Na2SO3+O2 =2Na2SO4������1������ɷ�ΪNa2SO3������2������ɷ�ΪNa2SO4����3��Na2SO3��Na2SO4��
��ʵ����ۡ�
��1��װ��ͼ������֪װ��A���Ƕ�����������ķ���װ�ã���Ӧ�Ļ�ѧ����ʽΪ��Na2SO3+H2SO4 =Na2SO4+H2O+SO2����
��2����A�з�Һ©���Ļ�������Ӧ����������������SO2�����ô����ǵ�ľ�������a�����������壬ľ����ȼ��˵�����������������������������Ӧ���ʲ���2����
��3��ˮ����������Ʒ�Ӧ����Ũ����ɸ������壬��ֹˮ�μӷ�Ӧ������B��Ũ��������Ϊ����SO2��D�пɷ�ֹ�������������ŷ��ڻ����кͷ�ֹ�����еĶ�����̼��ˮ��������C�У�
��4��������Na2SO3������Ϊx
2SO2+2Na2O2=2Na2SO3+O2��
156 252
78g x
![]()
x=126g
Na2SO4������Ϊ134g��126g=8g��
���ܽ�������
��1�����ַ�Ӧ��ȫ��ΪNa2SO3������Ϊy����ַ�Ӧ��ȫ��ΪNa2SO4������Ϊz
��2SO2+2Na2O2=2Na2SO3+O2��2Na2SO3+O2=2Na2SO4��֪��
Na2O2��Na2SO3��Na2SO4
78 126 142
m1 g y z
![]()
y=![]() g
g
z=![]() m1g
m1g
��m2��ȡֵ��Χ��![]() g��m2��
g��m2��![]() m1g
m1g
��2����ɫ�����к���Na2SO3������������ɴ̼������壬����Ʒ����ɫ֤��Ϊ������������鷽��Ϊ����ɫ��������ˮ���μ����ᣬ�ռ����壬������ͨ��Ʒ����Һ����Ʒ����ɫ����˵������Na2SO3������Ϊ�����ƣ�

 ��У����ϵ�д�
��У����ϵ�д�