题目内容
【题目】为了测定某黄铜![]() 铜锌合金
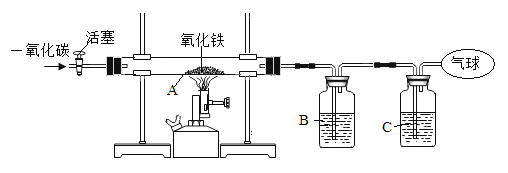
铜锌合金![]() 样品的组成,某化学兴趣小组的同学进行了以下实验:取四份相同质量的样品分别放入等质量的烧杯中,然后分别加入硫酸,充分反应后用天平称量,记录实验数据如下:
样品的组成,某化学兴趣小组的同学进行了以下实验:取四份相同质量的样品分别放入等质量的烧杯中,然后分别加入硫酸,充分反应后用天平称量,记录实验数据如下:
试验次序 | 第1次 | 第2次 | 第3次 | 第4次 |
所取样品的质量
|
|
|
|
|
加入稀硫酸的质量 |
|
|
|
|
生成气体的质量 |
|
|
|
|
请回答下列问题并计算:
![]() 经分析,在第1次实验结束后,反应物______完全反应完了。
经分析,在第1次实验结束后,反应物______完全反应完了。
![]() 样品与足量稀硫酸反应最多能生成气体______g
样品与足量稀硫酸反应最多能生成气体______g
![]() 计算样品中锌的质量分数
计算样品中锌的质量分数![]() 写出具体计算过程
写出具体计算过程![]() 。______
。______
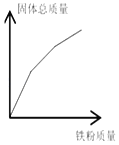
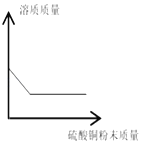
![]() 请在图中画出加入稀硫酸的质量与生成气体的质量的变化关系。______
请在图中画出加入稀硫酸的质量与生成气体的质量的变化关系。______

【答案】稀硫酸 0.5 32.5% 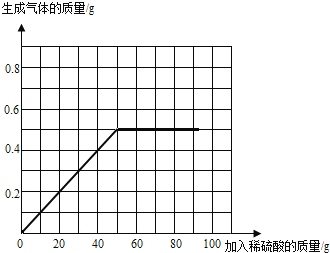
【解析】
(1)有题目给出的信息可知:第一、二次所取样品的质量相等的情况下,酸的质量增加生成氢气的质量也增加,说明在第一次中酸完全反应,样品中金属锌有剩余;故答案为:稀硫酸
(2)有题目给出的信息可知20g稀硫酸完全反应能生成0.2g氢气,所以若60g稀硫酸完全反应可生成0.6g氢气,而第三次中50g样品与60g稀硫酸充分反应只生成了0.5g氢气,说明样品完全反应酸有剩余,故50g样品与足量稀硫酸反应最多能生成氢气0.5g;故答案为:0.5。
(3)计算样品中锌的质量分数必须找一个样品完全反应生成的氢气的质量进行计算;故可根据第三次或第四次氢气的质量进行计算;
设50g样品中锌的质量为x
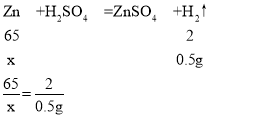
x=16.25g
样品中锌的质量分数为:![]() ×100%=32.5%
×100%=32.5%
答:样品中锌的质量分数为32.5%。
(4)加入稀硫酸的质量与生成气体的质量的变化关系图为:
 。
。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目