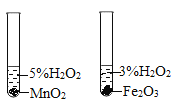题目内容
【题目】某兴趣小组进行铁生锈的实验探究活动。
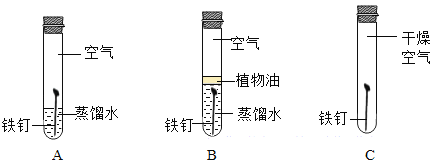
(探究一)铁生锈的条件
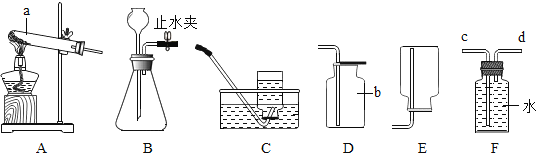
(1)该兴趣小组将洁净无锈的铁钉分别置于上图所示装置中,经过一段时间观察,_____(填序号)装置中出现了明显的锈迹。他们的结论是:铁生锈是因为铁与空气中的_____等发生了化学反应。
(2)卓玛同学提出疑问:空气中的氮气、二氧化碳没有参与铁的生锈过程吗?为卓玛同学释疑的实验可设计为:_____,观察并记录现象即可证明。
(探究二)影响铁生锈速率快慢的因素
拉姆说:妈妈常说菜刀沾有盐水生锈更快。这种说法对吗?
她查阅资料:导电性强(即离子浓度大)的溶液都可加速铁的生锈。
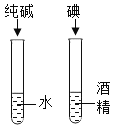
(3)将上述A装置中的蒸馏水改为下列液体中的_____(填序号),可使铁生锈速率加快。
a.硫酸钠溶液 b.无水乙醇
(4)酸性物质也能腐蚀钢铁,写出稀硫酸与铁反应的化学方程式_____。
【答案】A 氧气、水蒸气(化学式也可) 将A中的空气换为氮气或二氧化碳 a Fe+H2SO4=FeSO4+H2↑
【解析】
(1)铁生锈的条件是铁与空气中的水分和氧气共同作用的结果,A中铁钉满足铁生锈的条件,一段时间后会出现明显的锈迹;他们的结论是:铁生锈是因为铁与空气中的氧气、水蒸气(化学式也可)发生了化学反应;
(2)为卓玛同学释疑的实验可设计为:相同条件下将A中的空气换为氮气或二氧化碳,观察并记录现象即可证明;
(3)因为导电的溶液可加速铁的生锈,硫酸钠溶液中含有钠离子和硫酸根离子,如果把蒸馏水换为硫酸钠溶液可使铁生锈速率加快;而无水乙醇不导电,不能加快铁生锈的速率;
(4)稀硫酸与铁反应生成硫酸亚铁和氢气,反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑。

【题目】实验方案的设计是培养创新能力的重要途径。下列实验方案的设计能达到目的的是
A | B | C | D |
|
|
|
|
探究影响物质溶解性的因素 | 探究可燃物燃烧的条件 | 比较不同催化剂的催化效果 | 探究铁生锈的所有条件 |
A.AB.BC.CD.D
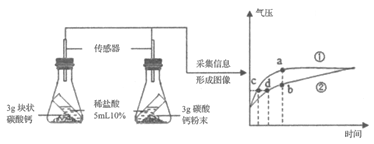
【题目】在学习金属的性质时,老师要求同学们根据实验室所提供的药品探究锌、铁、铜三种金属的活动性强弱。探究金属活动性强弱一般采用金属与酸的反应:根据能否与酸反应,以及与酸反应的剧烈程度来判断;于金属与化合物溶液的反应:根据能否将其置换出来,来判断金属的活动性强弱。
(提出问题)三种金属的活动性强弱是怎样的呢?
提供的药品有:铁粉、铜丝、锌粒、20%稀硫酸、CuSO4 溶液、ZnSO4 溶液、FeSO4 溶液
同学们分成甲、乙两组进行了实验。
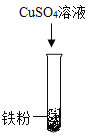
(1)甲组同学设计如下方案进行实验:
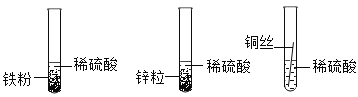
立刻有同学提出反对,理由是_____。
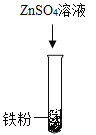
(2)乙组同学设计如下方案进行实验:
实验步骤 |
|
|
实验现象 | 无明显变化 | _____ |
实验结论 | 三种金属的活动性强弱为_____ | |
发生反应的化学方程式为_____。
(3)乙组同学将两支试管中的物质倒在一个洁净的烧杯中,充分反应后过滤,同学们又对滤渣的成分展开了探究。
(作出猜想)猜想一:滤渣中一定有铜 猜想二:_____
实验步骤 | 向滤渣中加入一定量稀硫酸 |
实验现象 | _____ |
实验结论 | 猜想二正确 |
此时经过以上实验后的滤液中一定含有_____(填化学式)。
(拓展延伸)通过学习同学们掌握了比较金属活动性强弱的正确方法,同时又选择了另一组试剂_____,验证了三种金属的活动性强弱。