题目内容
【题目】(6分)现有一包白色粉末,可能由NaCl、Na2SO4、Na2CO3、NaNO3、CuSO4中的一种或几种组成。现做如下实验:①取少量粉末,加水溶解得无色溶液;②另取少量粉末,滴加稀盐酸,无明显现象。请回答:
(1)由实验①可确定原粉末中一定没有__________;由实验②可确定原粉末中一定没有__________。
(2)为进一步确定原粉末的组成,取少量粉末按如下图所示进行实验(每步所加试剂均不同):
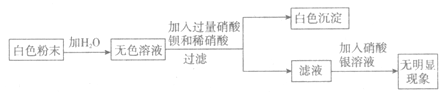
根据以上实验现象可知,原粉末中一定有的成分是__________,写出无色浴液与硝酸钡反应生的化学方程式:________________________________________。
(3)按照以上的探究过程及其现象,白色粉末的组成有__________种可能。
【答案】(1)CuSO4 Na2CO3(2)Na2SO4 ![]() (3)2
(3)2
【解析】
试题分析:加水溶解得无色溶液所以物质中不会含有硫酸铜;另取少量粉末,滴加稀盐酸,无明显现象说明不含有碳酸钠,溶液中加入硝酸钡会产生沉淀说明原粉末中一定有的成分是硫酸钠,硫酸钠和硝酸钡反应产生硫酸钡沉淀,该沉淀不溶于酸中,按照以上的探究过程及其现象,加入硝酸银没有沉淀产生说明不会含有氯化钠,因此白色粉末的组成可能是:硫酸钠;或者是硫酸钠和硝酸钠两种。

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目