题目内容
为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如下表:
试计算所用稀硫酸的溶质质量分数.
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加入稀硫酸质量(g) | 100 | 100 | 100 | 100 |
| 剩余固体质量(g) | 87 | 74 | 67.5 | 67.5 |
依据题意,第一次中参加反应的锌的质量为100g-87g=13g,设参加反应的H2SO4质量为x
Zn+H2SO4=ZnSO4+H2↑
65 98
13g x
=
x=19.6g
则所用稀硫酸的溶质质量分数=
×100%=19.6%
答:反应后所得溶液中溶质的质量分数为19.6%.
Zn+H2SO4=ZnSO4+H2↑
65 98
13g x
| 65 |
| 13g |
| 98 |
| x |
x=19.6g
则所用稀硫酸的溶质质量分数=
| 19.6g |
| 100g |
答:反应后所得溶液中溶质的质量分数为19.6%.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如下表:
试计算所用稀硫酸的溶质质量分数.
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加入稀硫酸质量(g) | 100 | 100 | 100 | 100 |
| 剩余固体质量(g) | 87 | 74 | 67.5 | 67.5 |
为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如下表:
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加入稀硫酸质量(g) | 100 | 100 | 100 | 100 |
| 剩余固体质量(g) | 87 | 74 | 67.5 | 67.5 |
为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如下表:
(1)第2次测得剩余固体质量为74g,其成分为______.
A.铜 B.锌 C.铜和锌
(2)该黄铜样品中铜和锌的质量比m铜:m锌:______.
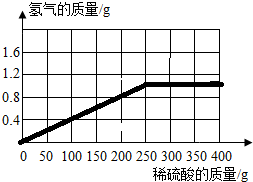
(3)计算所用稀硫酸的溶质质量分数,并画出反应生成的氢气质量与加入稀硫酸质量的关系图.______.
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加入稀硫酸质量(g) | 100 | 100 | 100 | 100 |
| 剩余固体质量(g) | 87 | 74 | 67.5 | 67.5 |
A.铜 B.锌 C.铜和锌
(2)该黄铜样品中铜和锌的质量比m铜:m锌:______.
(3)计算所用稀硫酸的溶质质量分数,并画出反应生成的氢气质量与加入稀硫酸质量的关系图.______.

为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如下表:
试计算所用稀硫酸的溶质质量分数.
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加入稀硫酸质量(g) | 100 | 100 | 100 | 100 |
| 剩余固体质量(g) | 87 | 74 | 67.5 | 67.5 |
 (2012?乐陵市二模)为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如下表:
(2012?乐陵市二模)为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如下表: