题目内容
【题目】现有MgCO3和BaCO3组成的固体混合物6g,放入到100g某浓度的稀盐酸中恰好完全反应,得到不饱和溶液的质量为103.8g,则原固体混合物中Mg、Ba两种元素的质量分数总和为_____。
【答案】50%
【解析】
碳酸镁与稀盐酸反应生成氯化镁、水和二氧化碳,碳酸钡与稀盐酸反应生成氯化钡、水和二氧化碳,根据质量守恒定律可以求得二氧化碳的质量,进一步计算固体混合物中碳酸根的质量,可以求解原固体混合物中Mg、Ba两种元素的质量分数总和。
根据质量守恒定律,二氧化碳的质量为6g+100g﹣103.8g=2.2g,根据MgCO3+2HCl═MgCl2+H2O+CO2↑,BaCO3+2HCl═BaCl2+H2O+CO2↑。
设:原固体混合物中碳酸根的质量为x
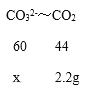
![]() x=3.0g
x=3.0g
则原固体混合物中Mg、Ba两种元素的质量为6g﹣3.0g=3.0g;原固体混合物中Mg、Ba两种元素的质量分数总和=![]() ×100%=50%
×100%=50%

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目