题目内容
【题目】下图示意的是教材上的三个实验,请回答:

(1)甲实验黄铜片和铜片互相刻画,出现划痕的是_________(填“黄铜片”或“铜片”)。
(2)乙实验中,左边试管内是铜丝放入硝酸银溶液中,反应的化学方程式是_______。右边试管内是铝丝放入硫酸铜溶液中,实验现象是________。
通过两个实验得到关于金属活动性顺序的结论是_________。
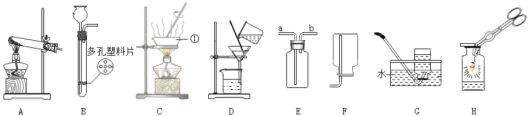
(3)丙是用水稀释浓硫酸的实验,盛放水的仪器叫________,玻璃棒不断搅拌的目的是______,证明硫酸溶于水的现象是______(填序号)。
A.放热 B.浓硫酸落于烧杯底部 C.最终得到均一的无色液体
【答案】铜片 2AgNO3+Cu=Cu(NO3)2+2Ag 铝丝表面有红色物质析出,溶液由蓝色变成无色 Al>Cu>Ag 烧杯 使热量迅速散失 AC
【解析】
(1)合金的硬度比组成其纯金属的硬度大,所以甲实验黄铜片和铜片互相刻画,出现划痕的是铜,故填铜片;
(2)铜和硝酸银反应生成硝酸铜和银,故化学方程式为:2AgNO3+Cu=Cu(NO3)2+2Ag;
铝和硝酸铜反应生成硝酸铝和铜,实验现象是:铝丝表面有红色物质析出,溶液由蓝色变成无色,故填铝丝表面有红色物质析出,溶液由蓝色变成无色;
通过两个实验得到关于金属活动性顺序的结论是:Al>Cu>Ag,故填Al>Cu>Ag;
(3)盛放水的仪器的名称是烧杯,故填烧杯;
稀释浓硫酸时,玻璃棒不断搅拌的目的是:使热量迅速散发,防止液滴向外飞溅,故填使热量迅速散发;
证明硫酸溶于水的现象是:放热,最终得到均一的无色液体,故选AC。

练习册系列答案
相关题目