题目内容
【题目】小亮同学在实验室中制取CO2气体后,对废液进行后续探究,他向一定质量的含CaCl2和HCl的废液中逐滴加入溶质质量分数为10%的Na2CO3溶液。实验过程中加入Na2CO3溶液 质量与产生沉淀或气体的质量关系如图1所示;加入Na2CO3溶液的质量与溶液的PH变化关系如图2所示,请根据图示回答下列问题:

(1)图1中b→c段表示生成______ (选填“气体”或“沉淀”)的过程;
(2)图1中c时,溶液中的溶质为______ (写化学式);
(3)图1中o→a段反应过程中溶液的PH变化情况可用图2中___________段表示。
【答案】 沉淀 NaC d→h
【解析】(1)向一定质量的含CaCl2和HCl的废液中逐滴加入溶质质量分数为10%的Na2CO3溶液,碳酸钠先与稀盐酸反应生成二氧化碳,当稀盐酸反应完全后,碳酸钠与氯化钙反应生成碳酸钙沉淀。故生成二氧化碳的质量为2.2g,生成沉淀的质量为5g,其中图1中b→c段表示生成沉淀的质量;(2)图1中c时,表示碳酸钠与氯化钙恰好完全反应,此时溶液中的溶质为碳酸钠与氯化钙反应生成的氯化钠,氯化钠表示为NaCl;(3)图1中o→a段反应过程是碳酸钠与稀盐酸的反应,随着碳酸钠的加入,溶液的酸性逐渐的减弱,pH逐渐变大,当到达a点,表示碳酸钠与稀盐酸恰好完全反应,溶液的pH=7,故图1中o→a段反应过程中溶液的PH变化情况可用图2中d→h段表示。

 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案【题目】CaO和NaOH固体的混合物,俗名“碱石灰”,实验室常用作干燥剂。碱石灰在空气中久置会吸收空气中的水和二氧化碳而变质。某实验小组为确定一瓶久置的碱石灰样品的成分,设计了如图所示实验流程。
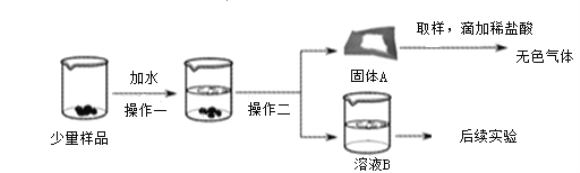
(1)固体A中一定含有____________。(写化学式)
(2)【问题与探究】过滤后滤液中会有哪些溶质?
【查阅资料】CaCl2溶液呈中性
【提出猜想】同学们提出以下猜想
①NaOH ②Na2CO3 ③NaOH和Na2CO3
④Ca(OH)2和________ ⑤NaOH、 Na2CO3 、Ca(OH)2
你认为该猜想________一定不正确,原因是_________________________________。
【实验与探究】
甲同学:取少量溶液B于试管中,滴加少许几滴稀盐酸,没有立即产生气泡,甲同学判断溶液B中的溶质一定没有Na2CO3。小红同学认为该同学结论不严密,因为_________________________________________________________________。
乙同学:取少量溶液B于试管中,滴加几滴Ca(OH)2溶液,看到______________现象,他认为B溶液中一定含有Na2CO3 。
为进一步帮助乙同学确认溶液B中是否含NaOH,你的实验设计是:
实验步骤 | 实验现象 | 实验结论 |
取无色溶液B少许于试管中,向其中加入____________溶液,过滤,再向滤液中加入______________________。 | ___________________ | 猜想③正确 |