题目内容
【题目】烧杯中盛有CuCl2和HCl的混合溶液100g,向其中滴加10%的NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示。下列说法正确的是
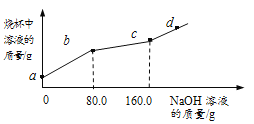
A. ab段反应产生蓝色沉淀
B. bc段溶液增加70.2g
C. c点对应的溶质质量分数为4.9%
D. d点溶液中溶质有2中,且PH>7
【答案】BD
【解析】烧杯中盛有CuCl2和HCl的混合溶液100g,向其中滴加10%的NaOH溶液,氢氧化钠先和稀盐酸反应生成氯化钠和水,当稀盐酸反应完后,再与氯化铜反应,生成氢氧化铜沉淀和氯化钠,据此分析判断。
A.由图像可知,ab段反应是氢氧化钠先和稀盐酸反应生成氯化钠和水,故错误;
B.由题意可知:与氯化铜反应的氢氧化钠的质量为:(160.0-80.0)g×10%=8.0g
设生成氢氧化铜的质量为x,生成氯化钠的质量为y。
CuCl2+2NaOH=Cu(OH) 2↓+2NaCl
80 98 117
8.0g x y
![]()
x=9.8g
y=11.7g
bc段溶液增加的质量为:80g-9.8g=70.2g。故B正确;
C.设氢氧化钠与盐酸反应生成氯化钠的质量为z。
HCl+NaOH=NaCl+H2O
40 58.5
80g z
![]()
z=11.7g
c点对应的溶质质量分数为:![]() =9.3%。故错误;
=9.3%。故错误;
D. d点溶液中溶质有过量的氢氧化钠和生成的氯化钠且PH>7,正确。

【题目】工业上采用氨碱法生产纯碱,主要流程如下图,请据图回答相关问题。
![]()
⑴氨碱法生产所得产品为纯碱,向纯碱水溶液中滴入无色酚酞试液显________色。
⑵从步骤①提取粗盐常用___________(填“蒸发结晶”或“降温结晶”)方法。
⑶从酸碱反应的角度分析,步骤④中通入氨气的作用是____________________。
⑷步骤⑤所得的碳酸氢钠在生产和生活中有许多重要用途,请写出它的一种用途______。
⑸步骤⑥中发生反应的化学方程式为______________,该反应类型属于________反应。
⑹工业产品中往往含有一些杂质,用“氨碱法”制得的纯碱含有少量氯化钠。为了测定该产品中碳酸钠的纯度,进行以下实验:取16.5g纯碱样品放入烧杯中,将烧杯放在电子天平上,再把150g稀盐酸(足量)加入样品中,观察读数变化如下表所示:
时间/s | 0 | 5 | 10 | 15 |
读数/g | 215.2 | 211.4 | 208.6 | 208.6 |
请你据此分析计算:
①实验中产生二氧化碳的质量为____________;
②该产品中碳酸钠的质量分数_______(写出计算过程,结果精确到0.1%)
【题目】下列化学方程式与对应反应类型均正确的是( )
化学方程式 | 反应类型 | |
A | Cu2(OH)2CO3 △ CuO+H20+CO2↑ | 分解反应 |
B | 4Al+3O2 === 2Al2O3 | 化合反应 |
C | 2Fe + 6HCl === 2FeCl3 + 3H2↑ | 置换反应 |
D | SO3 + 2NaOH === Na2SO4 + H2O | 复分解反应 |
A. A B. B C. C D. D