题目内容
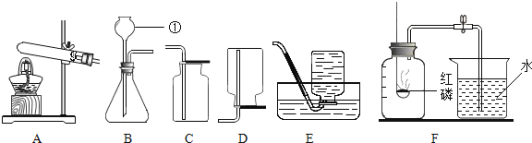
【题目】如图是a、b、c三种物质的溶解度曲线,下列说法正确的是

A. t2℃时三种物质的饱和溶液中溶质质量分数的大小关系是a>b>c
B. 等质量的a、b溶液降温后,析出晶体的质量一定是a>b
C. c可能为气体,它的饱和溶液变为不饱和溶液,可采用升温的方法
D. t2℃时,将30g a加入到50g水中,得到80g a的饱和溶液
【答案】A
【解析】
A、t2℃时,a物质的溶解度最大,b物质的溶解度次之,c物质的溶解度最小,所以三种物质的饱和溶液中溶质质量分数的大小关系是a>b>c,故A正确;
B、等质量的a、b溶液降温后,降到的温度不能确定,析出晶体的质量也不能确定,故B错误;
C、气体物质的溶解度随温度的升高而减小,所以c可能为气体,它的饱和溶液变为不饱和溶液,可采用降温的方法,故C错误;
D、t2℃时,a物质的溶解度是50g,所以将30ga加入到50g水中,只能溶解25g,得到75ga的饱和溶液,故D错误。
故选A。

 阅读快车系列答案
阅读快车系列答案【题目】如图所示,A~I是初中化学常见的物质,A的水溶液显碱性,D为大理石的主要成份,F为生活中最常见的调味剂,Y为红色固体,G与I组成元素相同,请根据图示回答下列问题(部分产物或反应条件省略):
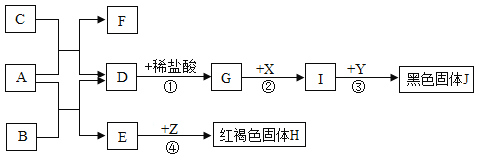
⑴A的俗名为_____;
⑵反应③的化学方程式为_____;
⑶反应④的可能化学方程式为_____;
⑷Y属于是_____(选填“混合物”、“单质”或“氧化物”);
⑸某化学兴趣小组对①反应的废液过滤后的成份产生了兴趣.进行了实验探究:
(提出问题)将废液过滤后,滤液中的溶质含有哪些物质?
(猜想与假设)猜想I:滤液中的溶质只有氯化钙;
猜想Ⅱ:滤液中的溶质有_____
(进行实验)①甲小组的同学从下面A-E五种药品中选择合适的一种进行实验,证明了猜想Ⅱ是正确的。他们选择的药品不可能是_____。
A 紫色石蕊试液 B无色酚酞试液 C 锌粒 D 氧化铁粉末 E 氢氧化钠溶液
②乙小组选用一种钠盐溶液进行实验,也证明了猜想Ⅱ是确的,请完成下面的实验报告。
实验操作 | 实验现象 | 实验结论 |
取少量滤液于试管中,加入足量_____(填化学式)溶液,振荡。 | _____ | 猜想Ⅱ正确 |
【题目】工业上以高纯度的二氧化锰为原料制备高锰酸钾的主要流程如下:
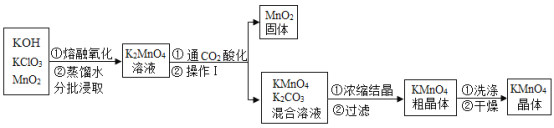
资料查阅:已知相关物质的溶解度(20℃)如下表
物质 | K2CO3 | K2SO4 | KMnO4 |
溶解度/g | 111 | 11.1 | 6.34 |
(1)KMnO4中锰元素的化合价为_____。上述流程中可循环利用的物质是_____
(2)“干燥”过程中温度不宜过高的原因是(用化学方程式表示)_____
(3)结合流程和有关信息,补充完整由KMnO4和K2CO3混合溶液中结晶得到KMnO4晶体的实验方案:蒸发浓缩、_____、过滤、洗涤、干燥。
(4)“通CO2酸化”,反应的化学方程式为:3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3,若用稀硫酸酸化,反应的化学方程式为:3K2MnO4+2H2SO4=2KMnO4+MnO2↓+2K2SO4+2X,则X的化学式为_____,工业上不采用稀硫酸酸化的的原因是_____