��Ŀ����
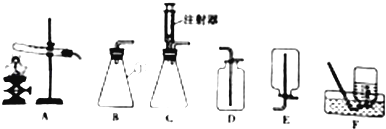
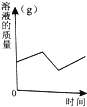
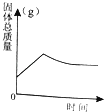
����Ŀ��ij��ѧ��ȤС���θҩ��̼������Ƭ��������̽���������������£�
��ȡ1Ƭθҩ���飬��ˮ��ȫ�ܽ�õ�100g��Һ��
������100g0.365%��ϡ������Ϊģ��θ�
��ȡ����һ����Һ20g����ƿ�У��ٽ���һ����Һ��μ�����ƿ�ڣ���Ӧ����Һ��pH�仯�����ͼ��ʾ��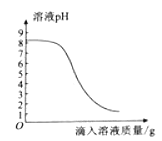
��ش��������⣺
��1��̼��������������ᡱ������Ρ�����
��2��������У���������һ����Һ������Ϊ10gʱ����ƿ������ǡ����ȫ��Ӧ��θҩ�������ɷֲ��μӷ�Ӧ���������ʵ�����ݼ���ÿƬθҩ��̼�����Ƶ�������д����Ҫ�ļ�����̣�
���𰸡�
��1����
��2��
��20g̼��������Һ�к��е�̼�����Ƶ�����Ϊx
NaHCO3+HCl=NaCl+H2O+CO2��
84 36.5
x 10g��0.365%
![]()
��ã�x=0.084g��
ÿƬθҩ��̼�����Ƶ�������0.084g�� ![]()
![]() =0.42g
=0.42g
��ÿƬθҩ��̼�����Ƶ�������0.42g��
���������⣺��1��̼��������������ͽ�����ɵģ������Σ�
��1������̼�����Ƶ���ɷ������ʵ���𣻣�2������̼������������ķ�Ӧ�������������ʵ����������20g̼��������Һ�к��е�̼�����Ƶ������������ÿƬθҩ��̼�����Ƶ�������������Ҫ���������ʵķ�����ݻ�ѧ����ʽ�ļ��㣬�ѶȲ��������е�֪ʶ������ɣ�

 ��Ч���ܿ�ʱ��ҵϵ�д�
��Ч���ܿ�ʱ��ҵϵ�д� �ݾ�ѵ������ϵ�д�
�ݾ�ѵ������ϵ�д�����Ŀ������ͭ��Һ�Թ�������ķֽ��д����ã�ȡһ������8.5%�Ĺ���������Һ�����ձ��У�����һ������15%������ͭ��Һ������������ȫ�ֽ⣬�й�ʵ�����������ʾ��������������ˮ�е��ܽ⣩������㣺
��Ӧǰ | ��Ӧ�� | ||
ʵ������ | �ձ�����������Һ������/g | ����ͭ��Һ������/g | �ձ����ձ�����Һ������/g |
60 | 3.3 | 62.5 | |
��1����������������Ϊg��
��2����Ӧ���ձ�����Һ���ʵ�������������д��������̣������ȷ��0.1%����