��Ŀ����
������һ�ַdz���Ҫ����Դ�������������������Ź㷺����;��
��1������ÿ�����Ȼ����ȡ�����Ľ�����������ȡ�������������ó�������Ҫ�ɷ�ΪFe2O3����һ����̼�����Ļ�ѧ����ʽΪ �� �� ��
��2��ÿ�������ϸ����IJ����ܸߣ���ȫ����ÿ����������ʧ�ĸ���Լռ��������������1/4�������������˾����ʧ�����ڿ�������ʴ��ʵ���������������е� �� ��ͬ���õĽ��������һ��������˿���Ѿ���ʼ���⣬�����û�ѧ�������⣬��������������Ҫд������������漰���Ļ�ѧ����ʽ���� ��
��3������ͬѧ��ϡ�������һ����Һ����֤��Mg��Fe��Cu��Ag���ֽ����Ļ��˳�������μ����ģ���ش��������⣺
���������õ���һ����Һ���� ����
��˵��Mg��Fe���õ�ʵ���������� ����
��˵��Cu��Ag���õ�ʵ���������� ����
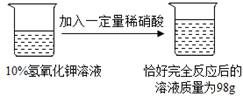
��4���ҹ��ڽ���ұ�����������ƾõ���ʷ�������ϱ���ʱ�ھͿ�ʼұ����ͭ����ͭ����ͭ��п��ɵģ���������������������������������Ʒ����Ϊ�ⶨij��ͭ��Ʒ��ͭ�ĺ�����ȡ�û�ͭ��Ʒ10g������100g��ϡ�����У�ǡ����ȫ��Ӧ����ʱ�ձ��ڸ����ʵ�������Ϊ109.8g���Լ��㣺
��1���û�ͭ��Ʒ��ͭ������������
��2����Ӧ����ϡ�������������������
��1��3CO+Fe2O3 2Fe+3CO2��2ˮ����������������ϡ���������������ʧ��Ȼ������ˮ��ϴ�ɾ��������Ϳ��Щ�ʹӶ����⣮Fe2O3+H2SO4=Fe2��SO4��3+3H2O��3������������Һ��������ͭ��Һ����ð�����ݵ����ʿ��ͭ˿������һ������ɫ�������ɣ�������������4��7.3%
2Fe+3CO2��2ˮ����������������ϡ���������������ʧ��Ȼ������ˮ��ϴ�ɾ��������Ϳ��Щ�ʹӶ����⣮Fe2O3+H2SO4=Fe2��SO4��3+3H2O��3������������Һ��������ͭ��Һ����ð�����ݵ����ʿ��ͭ˿������һ������ɫ�������ɣ�������������4��7.3%
���������������1��һ����̼���л�ԭ�ԣ��ڸ��������£������������е�����ԭ�������ʴ�Ϊ��3CO+Fe2O3 2Fe+3CO2��2��������������������е�ˮ��������ͬ���õĽ�������������ϡ�����ϡ���ᣬ�ʴ�Ϊ��ˮ����������������ϡ���������������ʧ��Ȼ������ˮ��ϴ�ɾ��������Ϳ��Щ�ʹӶ����⣮Fe2O3+H2SO4=Fe2��SO4��3+3H2O��3������þ����������ǰ�����ܺ�ϡ���ᷴӦ�����ҷ�Ӧ���ҵ���þ����ͭ���������ܺ����ᷴӦ��Ϊ֤���������Ľ������ǿ������ѡ����������Һ������ͭ��Һ���ʴ�Ϊ������������Һ��������ͭ��Һ����ð�����ݵ����ʿ��ͭ˿������һ������ɫ�������ɣ�������������
2Fe+3CO2��2��������������������е�ˮ��������ͬ���õĽ�������������ϡ�����ϡ���ᣬ�ʴ�Ϊ��ˮ����������������ϡ���������������ʧ��Ȼ������ˮ��ϴ�ɾ��������Ϳ��Щ�ʹӶ����⣮Fe2O3+H2SO4=Fe2��SO4��3+3H2O��3������þ����������ǰ�����ܺ�ϡ���ᷴӦ�����ҷ�Ӧ���ҵ���þ����ͭ���������ܺ����ᷴӦ��Ϊ֤���������Ľ������ǿ������ѡ����������Һ������ͭ��Һ���ʴ�Ϊ������������Һ��������ͭ��Һ����ð�����ݵ����ʿ��ͭ˿������һ������ɫ�������ɣ�������������
��4���⣺��������������Ϊ��10g+100g��109.8g=0.2g
���ͭ��п������Ϊx��ϡ���������ʵ�����Ϊy��
Zn+2HCl=ZnCl2+H2��
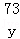
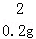
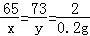
x=6.5g��y=7.3g
��ͭ��ͭ����������Ϊ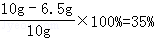
��Ҫ36.5%��Ũ��������Ϊ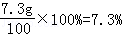
�𣺻�ͭ��ͭ����������35%�����õ�ϡ������������Ϊ7.3%��
���㣺�������˳����Ӧ�ã��й��������������ļ��㣻һ����̼��ԭ��������������ʴ�����������������Ļ�ѧ���ʣ���д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ�����ݻ�ѧ��Ӧ����ʽ�ļ��㣮

 100�ִ�����ĩ���ϵ�д�
100�ִ�����ĩ���ϵ�д� ��У���˿��ֿ���ϵ�д�
��У���˿��ֿ���ϵ�д���ѧС����ʵ�����ø��������ȡ����������һ��ʱ���ʣ����������Ϊ60g��Сϰͬѧ�������ȸù������������������ʱ�����ù�������Ϊ56��8g����ȴ����56��8g�����м�����ˮ�����˵õ�������Ϊ���������Ϊ17��4g��ʣ������м�Ԫ�صĺ���Ϊ���� �� ��
| A��25% | B��52% | C��50% | D��26% |
�����ۺ�ͭ�۵ľ��Ȼ����ס��ҡ�����λͬѧ�ֱ�ȡ�û������ϡ���ᷴӦ���������������ʾ��
| | �� | �� | �� |
| �������������/g | 10 | 10 | 20 |
| ϡ��������/g | 100 | 120 | 100 |
| ʣ���������/g | 4 | 4 | 13 |
��������ݣ��ش��������⣺
��1����ͬѧ������Һ�к��е������� ��
��2�������ͬѧ������Һ�����ʵ���������������������ȷ��0.1%��
ij��ȤС���ͬѧΪ�˲ⶨ̼������Ʒ��ֻ�����Ȼ��ƣ������������ʣ���̼���Ƶĺ�����ȡ�û������Ʒ������ϡ����ǡ����ȫ��Ӧ���й�ʵ�����ݼ�������
������ʵ������
| | ��Ӧǰ | ��Ӧ�� | |||
| ʵ������ | �ձ�������/g | ϡ���������/g | �������Ʒ������/g | �ձ������л���������/g | |
| 40.6 | 123.4 | 12 | 171.6 | | |
��2����Ʒ̼���Ƶ����������Ƕ��٣��������������0.1%��
��3����Ӧ��������Һ���������������Ƕ��٣�
(7��))����ʱ��ͬѧ�Dz����������ַ����ⶨij�Ȼ�����Һ����������������
��1������ѧ��������һ�����Ȼ�����Һ�м���������������Һ���õ�2.87g�Ȼ������壬����Ȼ�����Һ���Ȼ��Ƶ�����Ϊ���٣�(���ݻ�ѧ����ʽ��ʽ����)
�����ʵ��ⶨ������Һ��������������Ϊ10%��
��2��������������ȡһ��������Һ��������������ʵ���������£�
| �����������(g) | 25.0 |
| ������+ʳ����Һ(g) | 45.0 |
| ������+ʳ�ξ���(g) | 27.4 |
| ���ݴ��� | ��Һ��������������Ϊ |
A������ʱδ�ò���������
B����ȡ�Ȼ�����Һ�����ϴ�
C������ʱ������������ʱ��ֹͣ����
D��ʵ���δ���������ϵİ�ɫ��������������