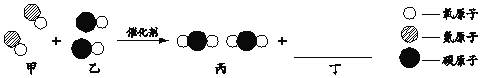题目内容
【题目】(6分)A是非金属,E是金属,B、C、D是化合物,它们之间有如下图所示的转化关系(反应条件已略去):

(1)在①②③④中,属于化合反应的是 (填序号)。
(2)反应①的化学方程式是 。
(3)在实验室里,反应①选择下图中的 (选填甲、乙、丙,下同)装置进行实验,反应②选择下图中的 实验。

【答案】(6分)
(1)③④ (2分,选两个且正确得2分,选一个且正确得1分,错选不得分)
(2)C+2CuO![]() 2Cu+CO2↑(2分) (3)丙(1分) 甲(1分)
2Cu+CO2↑(2分) (3)丙(1分) 甲(1分)
【解析】
红色物质E是铜单质,黑色单质A是炭,黑色化合物B是氧化铜,无色气体C是一氧化碳,无色气体D是二氧化碳;(1)④是炭与氧气反应生成二氧化碳属于化合反应,①是炭与氧化铜反应生成铜和二氧化碳不属于化合反应,③是一氧化碳与氧气反应生成二氧化碳属于化合反应,②是一氧化碳与氧化铜反应生成铜和二氧化碳,不属于化合反应,所以属于化合反应的是③④。
(2)反应①的化学方程式为C+2CuO![]() 2Cu+CO2↑
2Cu+CO2↑
(3)反应①是用炭还原氧化铜的反应,固固反应需要加热所以答案选丙。反应②是一氧化碳气体还原氧化铜的反应,所以答案选甲。

 阅读快车系列答案
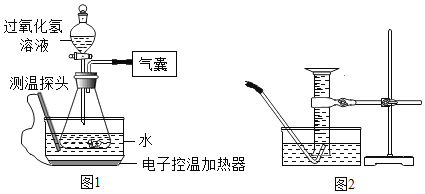
阅读快车系列答案【题目】某小组同学设计并进行实验,探究影响过氧化氢分解速率的因素.(实验装置如图1所示,夹持仪器已略去)
(猜想与假设)影响过氧化氢分解速率的因素可能有温度、溶液的浓度、催化剂种类.
(实验记录)同学们进行6组实验,实验记录如表:
实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
过氧化氢溶液的浓度(%) | 30 | 30 | 15 | 30 | 30 | 30 |
过氧化氢溶液的体积(mL) | 6 | x | 6 | 6 | 6 | 6 |
水槽中水的温度 | 20 | 90 | 70 | 70 | 20 | 20 |
锥形瓶中的物质 | ﹣﹣﹣﹣﹣ | ﹣﹣﹣﹣﹣ | ﹣﹣﹣﹣﹣ | ﹣﹣﹣﹣﹣ | 0.5gNaCl | 0.5gFeCl3 |
60min内产生氧气(mL) | 0.0 | 41.0 | 4.5 | 12.1 | 2.0 | 650.0 |
(解释与结论)
(1)实验②中应加入过氧化氢溶液的体积x是_____mL.
(2)实验①~⑥通过测定相同时间内产生氧气的体积来比较过氧化氢的分解速率,还可以通过测定_____来比较过氧化氢的分解速率.
(3)得出“过氧化氢溶液的浓度越大分解速率越大”结论所依据的实验是_____(填序号).
(4)通过实验①、②、④可得出的结论是_____.
(反思与评价)
(5)同学们认为实验室制氧气,应选择实验⑥而不选实验②的理由是_____(答两点).
(6)某同学改用如图2所示装置代替气囊完成实验②,正确的实验操作顺序是_____.
a.将导管伸入量筒,开启控温加热器,滴入过氧化氢溶液
b.开启控温加热器,将导管伸入量筒,滴入过氧化氢溶液
c.开启控温加热器,滴入过氧化氢溶液,待导管口有连续均匀气泡冒出时将导管伸入量筒.
【题目】小婧同学学习化学后知道,镁在氧气中燃烧会生成白色的氧化镁固体,该反应的化学方程式为__________;但她在空气中点燃镁条时,发现生成的白色固体中还夹杂着少量的淡黄色固体。
(提出问题)为什么会生成淡黄色固体?
(查阅资料)小婧查阅资料,记录了下列几种物质的颜色:
物质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 |
颜色 | 白色 | 白色 | 淡黄色 | 白色 |
其他同学认为不需要查询________的颜色,理由是__________。
(提出猜想)分析资料,小茜认为淡黄色固体可能是由镁与空气中的氮气反应生成的。
(实验探究)
实验操作 | 实验现象 | 实验结论和化学方程式 |
__________ | ______ | 小茜的猜想成立,化学方程式为 _________。 |