题目内容
为了测定某碳酸钠样品中杂质氯化钠的质量分数,李明同学进行了三次实验,反应的化学方程式为:Na2CO3+CaCl2===CaCO3↓+2NaCl。实验数据如下表:
| 编 号 | 第1次 | 第2次 | 第3次 |
| 所取固体样品的质量/g | 7 | 5 | 5 |
| 加入氯化钙溶液的质量/g | 50 | 50 | 75 |
| 反应后生成沉淀的质量/g | 4 | 4 | 4 |
完成下列计算:
(1)反应的碳酸钠样品中碳酸钠的质量是多少?
(2)加入氯化钙溶液的溶质质量分数是多少?
(3)碳酸钠样品中杂质氯化钠的质量分数是多少?
解:(1)由题意分析李明的实验数据可知,第2次恰好完全反应。
设反应的碳酸钠的质量为x,参加反应的氯化钙质量为y。
Na2CO3+CaCl2===CaCO3↓+2NaCl
106 111 100
x y 4 g
 =
=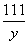 =
=
解得x=4.24 g,y=4.44 g
反应的碳酸钠样品中碳酸钠的质量是4.24 g
(2)加入的氯化钙溶液的溶质质量分数为: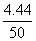 ×100%=8.88%
×100%=8.88%
(3)碳酸钠样品中杂质氯化钠的质量:5 g-4.24 g=0.76 g
其质量分数是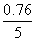 ×100%=15.2%
×100%=15.2%
答:(1)反应的碳酸钠样品中碳酸钠的质量是4.24 g;(2)加入氯化钙溶液的溶质质量分数是8.88%;(3)碳酸钠样品中杂质氯化钠的质量分数是15.2%。

 孟建平名校考卷系列答案
孟建平名校考卷系列答案为了测定某碳酸钠样品中杂质氯化钠的质量分数,李明同学进行了三次实验,反应的化学方程方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl.实验数据如下表:
| 编 号 | 第1次 | 第2次 | 第3次 |
| 所取固体样品的质量/g | 7 | 5 | 5 |
| 加入氯化钙溶液的质量/g | 50 | 50 | 75 |
| 反应后生成沉淀的质量/g | 4 | 4 | 4 |
(1)碳酸钠样品中碳酸钠的质量是多少?
(2)加入氯化钙溶液的溶质质量分数是多少?
(3)碳酸钠样品中杂质氯化钠的质量分数是多少?
为了测定某碳酸钠样品中杂质氯化钠的质量分数,李明同学进行了三次实验,反应的化学方程方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl。实验数据如下表:
| 编 号 | 第1次 | 第2次 | 第3次 |
| 所取固体样品的质量/g | 7 | 5 | 5 |
| 加入氯化钙溶液的质量/g | 50 | 50 | 75 |
| 反应后生成沉淀的质量/g | 4 | 4 | 4 |
完成下列计算:
(1)碳酸钠样品中碳酸钠的质量是多少?
(2)加入氯化钙溶液的溶质质量分数是多少?
(3)碳酸钠样品中杂质氯化钠的质量分数是多少?
为了测定某碳酸钠样品中杂质氯化钠的质量分数,李明同学进行了三次实验,反应的化学方程方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl。实验数据如下表:
| 编 号 | 第1次 | 第2次 | 第3次 |
| 所取固体样品的质量/g | 7 | 5 | 5 |
| 加入氯化钙溶液的质量/g | 50 | 50 | 75 |
| 反应后生成沉淀的质量/g | 4 | 4 | 4 |
完成下列计算:
(1)碳酸钠样品中碳酸钠的质量是多少?
(2)加入氯化钙溶液的溶质质量分数是多少?
(3)碳酸钠样品中杂质氯化钠的质量分数是多少?