题目内容
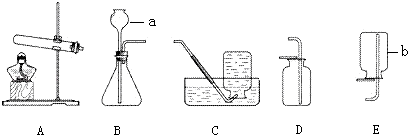
如图所示,是实验室制取O2、H2、CO2等气体的发生装置和收集装置,试回答:

(1)小明同学选择A装置准备用高锰酸钾为原料制取一瓶氧气,请你写出化学方程式 .
(2)小华同学想用过氧化氢(H2O2)溶液为原料,二氧化锰为催化剂代替高锰酸钾,制取并用排空气法收集一瓶氧气,她应选择的发生装置是 (填字母),理由是 , ,收集装置是 (填字母).
(3)你认为以上两种制取氧气的方法哪一种更好? .理由是 .
(4)上图中B装置还可制取 气体,你还需向实验老师领取的药品有 (写名称).

(1)小明同学选择A装置准备用高锰酸钾为原料制取一瓶氧气,请你写出化学方程式
(2)小华同学想用过氧化氢(H2O2)溶液为原料,二氧化锰为催化剂代替高锰酸钾,制取并用排空气法收集一瓶氧气,她应选择的发生装置是
(3)你认为以上两种制取氧气的方法哪一种更好?
(4)上图中B装置还可制取
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,二氧化碳的实验室制法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.用过氧化氢和二氧化锰制氧气比较好,因为本方法不需要加热,操作简便,节约能源等;实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.
解答:解:(1)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;故答案为:2KMnO4
K2MnO4+MnO2+O2↑
(2)如果用双氧水和二氧化锰制氧气就不需要加热,因为反应物是固体和液体,在常温下就能反应;因为制取并用排空气法收集一瓶氧气,氧气的密度比空气的密度大,因此用向上排空气法,故答案为:B;反应物是固体和液体;在常温下就能反应;E;
(3)用过氧化氢和二氧化锰制氧气比较好,因为本方法不需要加热,操作简便,节约能源等;故答案为:用过氧化氢和二氧化锰制氧气比较好;不需要加热,操作简便,节约能源;
(4)上图中B装置还可制取二氧化碳或氢气,因为实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,因此不需要加热,实验室是用锌粒和稀硫酸在常温下反应制氢气的,因此也不需要加热;故答案为:二氧化碳或氢气;石灰石和稀盐酸或锌粒与稀硫酸.
| ||
(2)如果用双氧水和二氧化锰制氧气就不需要加热,因为反应物是固体和液体,在常温下就能反应;因为制取并用排空气法收集一瓶氧气,氧气的密度比空气的密度大,因此用向上排空气法,故答案为:B;反应物是固体和液体;在常温下就能反应;E;
(3)用过氧化氢和二氧化锰制氧气比较好,因为本方法不需要加热,操作简便,节约能源等;故答案为:用过氧化氢和二氧化锰制氧气比较好;不需要加热,操作简便,节约能源;
(4)上图中B装置还可制取二氧化碳或氢气,因为实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,因此不需要加热,实验室是用锌粒和稀硫酸在常温下反应制氢气的,因此也不需要加热;故答案为:二氧化碳或氢气;石灰石和稀盐酸或锌粒与稀硫酸.
点评:本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和装置的优点等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
影响蔗糖在水中溶解的因素很多,当我们研究蔗糖颗粒大小对溶解快慢的影响时,需控制的影响因素有( )
| A、水量的多少 | B、温度的高低 |
| C、是否搅拌 | D、以上全部 |
下列实验操作正确的是( )
A、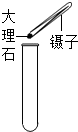 取用大理石 |
B、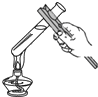 加热液体 |
C、 取少量液体 |
D、 称取氯化钠 |