题目内容
【题目】二氧化碳与氢氧化钠溶液反应没有明显现象,某兴趣小组设计如下图所示的实验装置,欲证明二氧化碳与氢氧化钠发生反应。
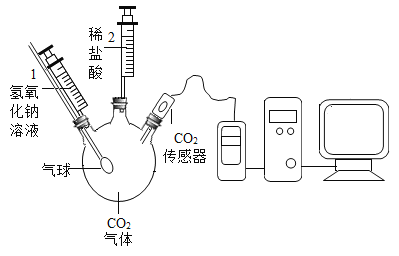
实验序号 | 实验操作 | 实验现象 |
① | 启动CO2传感器 | |
② | 将注射器1中的溶液推入充有CO2的瓶中 | 气球胀大 |
③ | 将注射器2中的溶液推入瓶中 | ________ |
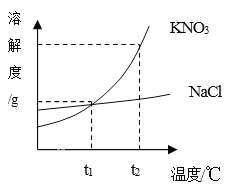
(1)实验是从定量的角度验证二氧化碳与氢氧化钠的反应,绘制曲线图象如图所示:
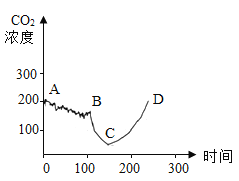
BC段发生反应的化学方程式为_________(假设氢氧化钠过量) ,CD段CO2浓度增大的原因是___________。
(2)实验结束后,向剩余的溶液中滴加酚酞溶液,发现溶液变成红色。同学们对这一现象产生了兴趣。
[提出问题]剩余溶液中,能使溶液呈碱性的物质是什么?
[猜想假设]小亮认为:只有碳酸钠
小红认为:只有氢氧化钠
小华认为:二者可能都有
[查阅资料]①同等条件下,中和反应优于酸和碳酸盐的反应
②氯化钙(或氯化钡)溶液呈中性
[交流讨论]同学们讨论后认为小红和小华的猜想均不成立。理由是__________。
[实验设计]小亮设计了如下实验,通过实验证明自己的猜想是正确的。
实验操作 | 实验现象 | 实验结论 |
①__________ | ________ | 小亮的猜想正确 |
②充分反应后,滴加几滴无色酚酞试液 | 溶液不变色 |
【答案】有气泡产生,气球缩小 ![]() 稀盐酸与实验②中生成的碳酸钠反应产生了CO2气体 实验③滴加的盐酸,会先和氢氧化钠反应完全后才和碳酸钠反应,所以剩余溶液中不可能有氢氧化钠(说法合理即可) 取剩余溶液少许于试管中,滴加足量(或过量)的CaCl2溶液(或BaCl2溶液) 有白色沉淀生成
稀盐酸与实验②中生成的碳酸钠反应产生了CO2气体 实验③滴加的盐酸,会先和氢氧化钠反应完全后才和碳酸钠反应,所以剩余溶液中不可能有氢氧化钠(说法合理即可) 取剩余溶液少许于试管中,滴加足量(或过量)的CaCl2溶液(或BaCl2溶液) 有白色沉淀生成
【解析】
[实验步骤]将注射器1中的氢氧化钠推入充有CO2的瓶中氢氧化钠和二氧化碳发生反应生成碳酸钠和水,将注射器2中的盐酸推入瓶中碳酸钠和盐酸反应生成二氧化碳和氯化钠和水,有气体生成,气压变大气球缩小,故填:有气泡产生,气球缩小。
(1)BC段氢氧化钠和二氧化碳反应生成碳酸钠和水,所以二氧化碳浓度减小,化学方程式为![]() ,CD段稀盐酸与实验②中生成的碳酸钠反应,产生了CO2气体,所以二氧化碳浓度增大,故填:
,CD段稀盐酸与实验②中生成的碳酸钠反应,产生了CO2气体,所以二氧化碳浓度增大,故填:![]() ;稀盐酸与实验②中生成的碳酸钠反应产生了CO2气体,所以二氧化碳浓度增大。
;稀盐酸与实验②中生成的碳酸钠反应产生了CO2气体,所以二氧化碳浓度增大。
(2)[交流讨论]实验③滴加的盐酸,会先和氢氧化钠反应,反应完全后才和碳酸钠反应,所以剩余溶液中不可能有氢氧化钠,小红和小华的猜想均不成立,故填:实验③滴加的盐酸,会先和氢氧化钠反应完全后才和碳酸钠反应,所以剩余溶液中不可能有氢氧化钠。
[实验设计]反应后,取剩余溶液少许于试管中,滴加足量(或过量)的CaCl2溶液(或BaCl2溶液),有白色沉淀生成说明剩余液体含碳酸钠,充分反应后,滴加几滴无色酚酞试液,溶液不变色,说明不含氢氧化钠,故填:取剩余溶液少许于试管中,滴加足量(或过量)的CaCl2溶液(或BaCl2溶液);有白色沉淀生成。

【题目】了解日用化工品的成分,有利于我们正确使用。
名称 | 洗洁精 | 炉具清洁剂 | 洁厕灵 | “84”消毒液 |
有效成分 | 表面活性剂 | 氢氧化钠 | 盐酸 | 次氯酸钠 |
(1)洗洁精能清洗餐具上的油污,是因为它具有______功能。
(2)炉具清洁剂的pH___7(填“>”“<”“或“=”)。使用时禁止与皮肤接触是因为氢氧化钠___性.
(3)不能用洁厕灵清洗铁制品的原因是______(用化学方程式表示)。
(4)洁厕灵与“84”消毒液不能混合使用,因为两者混合会发生反应:![]() ,生成的气体X有毒。X的化学式为____。
,生成的气体X有毒。X的化学式为____。