题目内容
28、对比实验是学习化学其中一种很重要的方法,请细心分析硫燃烧的几个步骤,说明物质燃烧与哪些因素有关.
| 实验操作 | 现象 | 相关解释 |
| 1.在燃烧匙里放入少量硫 | 无明显现象 | |
| 2.加热直到发生燃烧 | ||
| 3.把盛有燃着的硫的燃烧匙伸进充满氧气的集气瓶里 |
分析:了解物质燃烧所需要的三个条件,即物质具有可燃性、达到着火点、与氧气接触.了解硫燃烧的现象,并能做出相关解释.
(1)在燃烧匙中放入硫,未达到着火点;
(2)加热达到着火点可以燃烧,发出火焰,有刺激性气味产生;
(3)氧气有助燃作用,可是硫燃烧的更加剧烈.
(1)在燃烧匙中放入硫,未达到着火点;
(2)加热达到着火点可以燃烧,发出火焰,有刺激性气味产生;
(3)氧气有助燃作用,可是硫燃烧的更加剧烈.
解答:解:物质的燃烧所需要的条件是:物质具有可燃性、达到着火点、与氧气接触.
(1)在燃烧匙内放入少量硫,它不会燃烧,因虽是可燃物,但没有达到着火点;
(2)加热燃烧匙内的硫,因加热使硫达到着火点,硫开始燃烧.硫在空气中燃烧产生刺激性气味的气体,发出淡蓝色的火焰;(3)氧气有助燃的作用,所以、把盛有燃着的硫的燃烧匙伸进充满氧气的集气瓶里,硫剧烈燃烧,发出蓝紫色的火焰,并生成一种刺激性气味的气体.故表格内容如下:
(1)在燃烧匙内放入少量硫,它不会燃烧,因虽是可燃物,但没有达到着火点;
(2)加热燃烧匙内的硫,因加热使硫达到着火点,硫开始燃烧.硫在空气中燃烧产生刺激性气味的气体,发出淡蓝色的火焰;(3)氧气有助燃的作用,所以、把盛有燃着的硫的燃烧匙伸进充满氧气的集气瓶里,硫剧烈燃烧,发出蓝紫色的火焰,并生成一种刺激性气味的气体.故表格内容如下:
| 实验操作 | 现象 | 相关解释 |
| 1、在燃烧匙里放入少量硫 | 无明显现象 | 硫不能燃烧,因未达到硫的着火点 |
| 2、加热直到发生燃烧 | 硫燃烧,发出淡蓝色的火焰,生成一种有刺激性气味的气体 | 硫能燃烧,因硫加热后达到硫的着火点 |
| 3、把盛有燃着的硫的燃烧匙伸进充满氧气的集气瓶里 | 硫剧烈燃烧,发出蓝紫色的火焰,并生成一种刺激性气味的气体 | 硫剧烈燃烧,因氧气的浓度比空气中的氧气浓度高 |
点评:本题通过对比试验的形式,考查物质燃烧的条件,加深学生对燃烧条件的认识.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
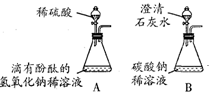

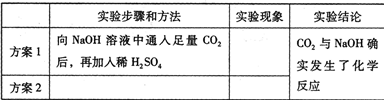
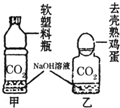
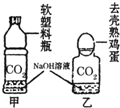 (2008?衡阳)实验室检验CO2通常用澄清石灰水,而吸收CO2通常用NaOH溶液,但CO2与NaOH溶液反应时无明显现象.振衡中学研究性学习小组就如何证明CO2与NaOH溶液确实发生了化学反应进行探究.
(2008?衡阳)实验室检验CO2通常用澄清石灰水,而吸收CO2通常用NaOH溶液,但CO2与NaOH溶液反应时无明显现象.振衡中学研究性学习小组就如何证明CO2与NaOH溶液确实发生了化学反应进行探究.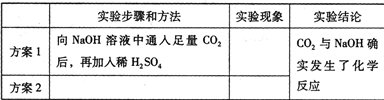
 实验室检验CO2通常用澄清石灰水,而吸收CO2通常用NaOH溶液,但CO2与NaOH溶液反应时无明显现象.振衡中学研究性学习小组就如何证明CO2与NaOH溶液确实发生了化学反应进行探究.
实验室检验CO2通常用澄清石灰水,而吸收CO2通常用NaOH溶液,但CO2与NaOH溶液反应时无明显现象.振衡中学研究性学习小组就如何证明CO2与NaOH溶液确实发生了化学反应进行探究.