题目内容
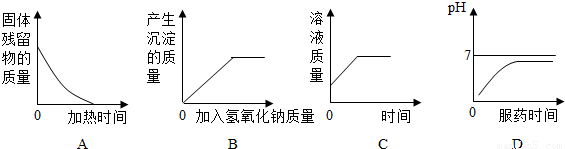
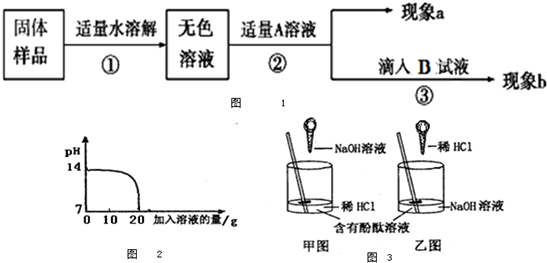
下列图象表示盐酸和氢氧化钠溶液发生反应过程中溶液的pH变化.请从图象中获取信息,回答下列问题:
(1)进行该反应的实验操作是按照以上______(填甲或乙)图所示进行,烧杯中溶液的颜色变化是______.
(2)所发生的中和反应的化学方程式为______.
(3)曲线上C点表示______.
(4)用溶质的质量分数为36.5%的盐酸40g与足量氢氧化钠溶液恰好完全反应,需要溶质的质量分数为20%的氢氧化钠溶液______g.
【答案】分析:氢氧化钠溶液呈碱性,其PH大于7,盐酸呈酸性,其PH小于7,氢氧化钠溶液和盐酸可以发生中和反应生成氯化钠和水,恰好完全反应时其PH等于7,氢氧化钠过量时显碱性,盐酸过量时显酸性.酚酞在碱性溶液中为红色,在中性和酸性溶液中为无色.
解答:解:(1)由图象可以看出,开始时溶液的PH大于7,呈碱性,表明是向氢氧化钠溶液中加入的盐酸,酚酞在碱性溶液中为红色,在中性和酸性溶液中为无色,所以本题答案为:乙,由红色变为无色;
(2)氢氧化钠溶液和盐酸可以发生中和反应生成氯化钠和水,所以本题答案为:HCl+NaOH═NaCl+H2O;
(3)C点对应的PH等于7,表明二者恰好完全反应,所以本题答案为:盐酸和氢氧化钠刚好完全中和,此时溶液pH为7(答案合理即可)
(4)设需要溶质的质量分数为20%的氢氧化钠溶液质量为x,
HCl+NaOH═NaCl+H2O
36.5 40
40g×36.5% x×20%
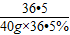 =
=
x=80g
答:需要溶质的质量分数为20%的氢氧化钠溶液80g.
点评:本题以图象的形式考查了酸碱中和反应时溶液PH的变化,以及物质间的质量关系,完成此题,可以依据已有的知识进行.
解答:解:(1)由图象可以看出,开始时溶液的PH大于7,呈碱性,表明是向氢氧化钠溶液中加入的盐酸,酚酞在碱性溶液中为红色,在中性和酸性溶液中为无色,所以本题答案为:乙,由红色变为无色;
(2)氢氧化钠溶液和盐酸可以发生中和反应生成氯化钠和水,所以本题答案为:HCl+NaOH═NaCl+H2O;
(3)C点对应的PH等于7,表明二者恰好完全反应,所以本题答案为:盐酸和氢氧化钠刚好完全中和,此时溶液pH为7(答案合理即可)
(4)设需要溶质的质量分数为20%的氢氧化钠溶液质量为x,
HCl+NaOH═NaCl+H2O
36.5 40
40g×36.5% x×20%
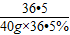 =
=
x=80g
答:需要溶质的质量分数为20%的氢氧化钠溶液80g.
点评:本题以图象的形式考查了酸碱中和反应时溶液PH的变化,以及物质间的质量关系,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目

 Na2CO3+CO2↑+H2O;③NaHCO3+HCl═NaCl+CO2↑+H2O;④少量的NaHCO3与Ca(OH)2反应:NaHCO3+Ca(OH)2=CaCO3↓+NaOH+H2O
Na2CO3+CO2↑+H2O;③NaHCO3+HCl═NaCl+CO2↑+H2O;④少量的NaHCO3与Ca(OH)2反应:NaHCO3+Ca(OH)2=CaCO3↓+NaOH+H2O
 Na2CO3+CO2↑+H2O;③NaHCO3+HCl═NaCl+CO2↑+H2O;④少量的NaHCO3与Ca(OH)2反应:NaHCO3+Ca(OH)2=CaCO3↓+NaOH+H2O
Na2CO3+CO2↑+H2O;③NaHCO3+HCl═NaCl+CO2↑+H2O;④少量的NaHCO3与Ca(OH)2反应:NaHCO3+Ca(OH)2=CaCO3↓+NaOH+H2O