题目内容
【题目】鸡蛋壳的主要成分是碳酸钙。为了测定某鸡蛋壳中碳酸钙的质量分数,小群同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取10g放在烧杯里,然后往烧杯中加入稀盐酸90g,恰好完全反应后,称得反应剩余物为97.14g。(假设蛋壳中的其他物质不与盐酸反应,也不溶于水。)
(1)产生二氧化碳气体______g。
(2)计算该鸡蛋壳中碳酸钙的质量分数______。
(3)计算反应后所得溶液溶质质量分数________。
【答案】2.86g 65% 7.7%
【解析】
(1)据质量守恒定律可知反应前后物质的总质量不变,产生二氧化碳气体的质量为:10g+90g-97.14g =2.86g;
(2)设该鸡蛋壳中碳酸钙的质量为x,生成氯化钙的质量为y
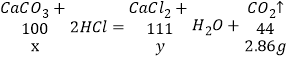
![]()
x=6.5g ![]() =65%
=65%
答:鸡蛋中碳酸钙的质量分数为65%
(3) ![]() y=7.215g
y=7.215g
反应后所得溶液溶质质量分数:
![]() ≈7.7%
≈7.7%

 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案【题目】同学们发现新鲜的苹果汁在空气中放置一段时间后会变色,仿佛铁生锈一样。于是,研究性小组同学设计并进行实验,探究苹果汁变色的原因。
(查阅资料)
a.苹果汁中含有0.001%的二价铁物质,同时也含有多酚类物质,多酚可与空气中的氧气反应变为褐色。
b.二价铁在空气中或与浓硝酸反应都能变为三价铁,且三价铁的溶液为黄色
c.硫氰化钾(KSCN)溶液变色规律
药品 | 二价铁溶液 | 三价铁溶液 |
KSCN溶液 | 不变色 | 变红色 |
(猜想与假设)
Ⅰ.苹果汁变色与苹果中的铁元素有关
Ⅱ.苹果汁变色是苹果汁中的多酚物质与空气中的氧气反应的结果
(进行实验)
编号 | 实验操作 | 实验现象 | |||
实验1 |
| 试管②中未出现明显变化 试管③中…… | |||
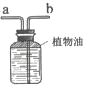
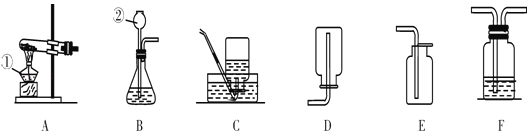
实验2 | 分别放置于空气中一段时间 (如下图所示)
| 试管编号 | 1min | 10min | 24小时 |
① | 黄褐色 | 褐色 | 深褐色 | ||
② | 无明显变化 | 无明显变化 | 无明显变化 | ||
③ | 略有些黄色 | 浅黄 | 黄色 | ||
实验3 | …… | 苹果汁不变色 | |||
(解释与结论)
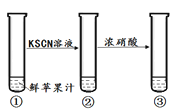
(1)实验1验证了苹果汁中含有二价铁物质。在该实验中③的现象是_____。
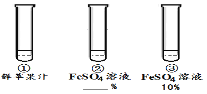
(2)实验2的②中FeSO4溶液溶质的质量分数为_____%。该实验中,试管②③实验对比得出的结论是_____。由实验2得出:猜想Ⅰ_____(填“成立”或“不成立”)。
(3)为验证猜想II成立,实验3应进行的操作_____。
(反思与评价)
(4)写出一种防止苹果汁变色的方法_____。