题目内容
海洋是一个巨大的资源宝库,我们可以从海水中提取氯化钠,并以氯化钠为原料制得氢氧化钠、氢气和氯气(Cl2).其制取的主要工艺流程如下: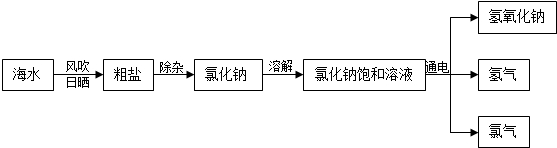
(1)利用风吹日晒可以从海水中提取粗盐,得到粗盐后要进行精制.实验室要除去食盐水中混有少量的泥沙,选择的操作方法是 .在该操作中用到的玻璃仪器除烧杯、漏斗外,还需要 ,其作用是 .
(2)若用10%的氯化钠溶液稀释成100g0.9%的氯化钠溶液,需要10%的氯化钠溶液 g.
(3)氯化钠饱和溶液在通电条件下发生反应的化学方程式是: .

(1)利用风吹日晒可以从海水中提取粗盐,得到粗盐后要进行精制.实验室要除去食盐水中混有少量的泥沙,选择的操作方法是
(2)若用10%的氯化钠溶液稀释成100g0.9%的氯化钠溶液,需要10%的氯化钠溶液
(3)氯化钠饱和溶液在通电条件下发生反应的化学方程式是:
分析:(1)根据混合物分离的方法分析;
(2)根据溶液稀释前后溶质质量不变分析
(3)根据电解饱和食盐水时,能生成氢氧化钠、氢气和氯气进行解答.
(2)根据溶液稀释前后溶质质量不变分析
(3)根据电解饱和食盐水时,能生成氢氧化钠、氢气和氯气进行解答.
解答:解:(1)因为泥沙不溶于水,而氯化钠溶于水,所以可以采用过滤的方法滤去泥沙,操作中用到的玻璃仪器除烧杯、漏斗外,还需要 玻璃棒,其作用是引流粗盐水.
(2)溶液加水稀释前后溶质质量不变,设需要10%的氯化钠溶液的质量为x,x×10%=100g×0.9%
x=9g
(3)氯化钠饱和溶液在通电条件下发生反应生成氢氧化钠、氢气和氯气,化学方程式为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑
故答案为:(1)过滤. 玻璃棒,引流.
(2)9.
(3)2NaCl+2H2O
2NaOH+H2↑+Cl2↑.
(2)溶液加水稀释前后溶质质量不变,设需要10%的氯化钠溶液的质量为x,x×10%=100g×0.9%
x=9g
(3)氯化钠饱和溶液在通电条件下发生反应生成氢氧化钠、氢气和氯气,化学方程式为:2NaCl+2H2O
| ||
故答案为:(1)过滤. 玻璃棒,引流.
(2)9.
(3)2NaCl+2H2O
| ||
点评:本题主要考查蒸发、溶解、化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目