题目内容
某化学实验兴趣小组在实验室进行实验,实验台上有酚酞和氯化钠两种溶液,老师要求同学们用实验台上的药品鉴别食盐水、纯碱溶液和澄清石灰水三种溶液,实验后的废液都倒入一个干净的废液缸中,正确进行实验后,同学们发现废液缸中的液体呈红色,废液缸体都有少量白色沉淀.
【提出问题】沉淀一定是碳酸钙,废液中除水和酚酞外,还含有哪些物质?
【作出猜想】经过讨论,大家一致认为:废液中一定有氯化钠,可能有氢氧化钠、碳酸钠和氢氧化钙中的一种或几种.
为了进一步确定该废液中含有的物质,作如下探究:
【进行实验】小明同学利用实验台上的药品进行实验(补全表格中的内容)
【实验分析】小明同学针对自己的实验推理得出:
(1)废液中一定不含 ,得出此结论的理由是
(2)废液中还一定含有
【反思拓展】在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑 .
【提出问题】沉淀一定是碳酸钙,废液中除水和酚酞外,还含有哪些物质?
【作出猜想】经过讨论,大家一致认为:废液中一定有氯化钠,可能有氢氧化钠、碳酸钠和氢氧化钙中的一种或几种.
为了进一步确定该废液中含有的物质,作如下探究:
【进行实验】小明同学利用实验台上的药品进行实验(补全表格中的内容)
| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液中的上层清液于试管中 | 废液中含有碳酸钠,发生反应的化学方程式是 |
(1)废液中一定不含
(2)废液中还一定含有
【反思拓展】在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑
考点:实验探究物质的组成成分以及含量,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:纯碱是碳酸钠的俗称,能和石灰水中的氢氧化钙反应生成碳酸钙沉淀和氢氧化钠;
【进行实验】
碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳;
【实验分析】
氢氧化钙和碳酸钠不能共存;
氢氧化钙和碳酸钠反应生成的氢氧化钠不能和溶液中的其它物质发生化学反应;
反应物之间按照一定的质量比进行反应时,可能是恰好完全反应,也可能是有的反应物过量.
【进行实验】
碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳;
【实验分析】
氢氧化钙和碳酸钠不能共存;
氢氧化钙和碳酸钠反应生成的氢氧化钠不能和溶液中的其它物质发生化学反应;
反应物之间按照一定的质量比进行反应时,可能是恰好完全反应,也可能是有的反应物过量.
解答:解:【进行实验】
实验内容:取少量废液中的上层清液于试管中,滴加适量的稀盐酸;
预计现象:产生气泡;
预计结论:废液中含有碳酸钠,发生反应的化学方程式是:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
故填:滴加适量的稀盐酸;产生气泡;Na2CO3+2HCl═2NaCl+H2O+CO2↑.
【实验分析】
(1)因为氢氧化钙和碳酸钠不能共存,既然溶液中含有碳酸钠,则废液中一定不含氢氧化钙.
故填:氢氧化钙;氢氧化钙和碳酸钠不能共存.
(2)因为碳酸钠和氢氧化钙反应生成了氢氧化钠,所以废液中还一定含有氢氧化钠.
故填:氢氧化钠.
【反思拓展】
在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑反应物是否过量.
故填:反应物是否过量.
实验内容:取少量废液中的上层清液于试管中,滴加适量的稀盐酸;
预计现象:产生气泡;
预计结论:废液中含有碳酸钠,发生反应的化学方程式是:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
故填:滴加适量的稀盐酸;产生气泡;Na2CO3+2HCl═2NaCl+H2O+CO2↑.
【实验分析】
(1)因为氢氧化钙和碳酸钠不能共存,既然溶液中含有碳酸钠,则废液中一定不含氢氧化钙.
故填:氢氧化钙;氢氧化钙和碳酸钠不能共存.
(2)因为碳酸钠和氢氧化钙反应生成了氢氧化钠,所以废液中还一定含有氢氧化钠.
故填:氢氧化钠.
【反思拓展】
在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑反应物是否过量.
故填:反应物是否过量.
点评:实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
下列说法错误的是( )
| A、利用化学人类可以合成自然界不存在的物质 |
| B、研制设苗的过程中,化学将起到十分重要的作用 |
| C、化学工业给人类带来的只有益处没有害处 |
| D、利用化学可以研究和开发新能源 |
 如图是一种家用电热水壶,看图回答下列问题.
如图是一种家用电热水壶,看图回答下列问题.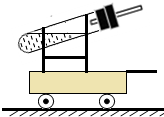 自制一个不使用电力的四轮小车(如图),往试管中加入化学试剂,塞紧塞子,让小车在摩擦力很小的水平道路上运动.
自制一个不使用电力的四轮小车(如图),往试管中加入化学试剂,塞紧塞子,让小车在摩擦力很小的水平道路上运动. 工业上用碳酸钠溶液与石灰水反应制烧碱,对于碳酸钠溶液与石灰水是否恰好完全反应,某化学兴趣小组的同学将其产物进行过滤,并对滤液进行如下探究.
工业上用碳酸钠溶液与石灰水反应制烧碱,对于碳酸钠溶液与石灰水是否恰好完全反应,某化学兴趣小组的同学将其产物进行过滤,并对滤液进行如下探究.