题目内容
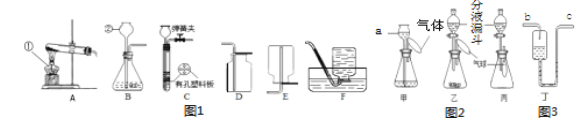
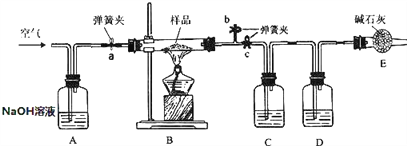
【题目】实验室现有一种含有纯碱、小苏打的固体粉末样品.为了测定其中小苏打的含量,某化学兴趣小组的同学在老师的指导下,利用如下图所示装置(部分固定装置已略去)进行实验.加热条件下,纯碱稳定不分解,小苏打易分解,反应的化学方程式为:2NaHCO3 ![]() Na2CO3+CO2↑+H2O。碱石 灰是 CaO 与 NaOH 的固体混合物;已知,该装置气密性良好,A、C、D 中所装药品足量且能完全吸收 相关物质.探究过程如下:
Na2CO3+CO2↑+H2O。碱石 灰是 CaO 与 NaOH 的固体混合物;已知,该装置气密性良好,A、C、D 中所装药品足量且能完全吸收 相关物质.探究过程如下:
Ⅰ.称量样品和已装入相关药品的 C、D 质量,分别为:m、mC1、,mD1.
Ⅱ.将质量为 m 的样品装入 B 玻璃管中,按图连接好装置,进行操作 X.
Ⅲ.关闭弹簧夹 a、b,打开弹簧夹 c,给玻璃管加热.
Ⅳ.待玻璃管中样品完全反应,打开弹簧夹 a 通入空气,再熄灭酒精灯,直到玻璃管冷却. Ⅴ.再次称量 C、D 的质量,分别为 mC2、mD2.请回答下列问题:
(1)步骤Ⅱ中操作 X 具体为____;
(2)C 中所装药品为____;
(3)D 中发生反应的化学方程式为____;
(4)步骤Ⅳ打开弹簧夹 a 通入空气,再熄灭酒精灯,直到玻璃管冷却的多重作用是____;
(5)依据实验实际,选择实验所得数据,该样品中小苏打含量的表达式为____.
【答案】 关闭弹簧夹 c,打开弹簧夹 a、b,并通入空气 浓硫酸 CO2+Ca(OH)2═CaCO3↓+H2O 防止倒吸,炸裂瓶底,使碳酸氢钠分解产生的二氧化碳尽量全部被D吸收等 将残留的 CO2 与水蒸气赶走或防倒吸![]()
【解析】一种含有纯碱、小苏打的固体粉末样品,测定其中小苏打的含量。(1)步骤Ⅱ中操作 X 具体为关闭弹簧夹 c,打开弹簧夹 a、b,并通入空气。(2)C 中所装药品为浓硫酸,浓硫酸具有吸水性,可以干燥酸性或中性气体。(3)D中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O。(4)步骤Ⅳ打开弹簧夹 a 通入空气,再熄灭酒精灯,直到玻璃管冷却的多重作用是防止倒吸,炸裂瓶底,使碳酸氢钠分解产生的二氧化碳尽量全部被D吸收。(5)依据实验实际,选择实验所得数据,该样品中小苏打含量的表达式为![]() 。
。
点睛∶纯碱稳定不分解,小苏打受热易分解。碱石灰是 CaO 与 NaOH 的固体混合物,可以干燥碱性或中性气体。

 阅读快车系列答案
阅读快车系列答案