题目内容
【题目】一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,下列说法不正确的是( )
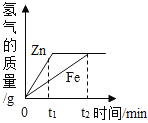
A.0﹣t1时段,产生氢气的质量锌比铁大
B.0﹣t1时段,产生氢气的速率锌比铁大
C.0﹣t2时段,参加反应的锌的质量与铁相同
D.0﹣t2时段,锌、铁消耗的盐酸质量相同
【答案】C
【解析】A、由图可知,0﹣t1时段,产生氢气的质量曲线锌在铁的上方,即锌的比铁的多,故A正确;
B、由图可知,0﹣t1时段,锌的反应曲线斜率比铁大,所以产生氢气的速率锌比铁大,故B正确;
C、0﹣t2时段产生的氢气相等,而反应中生成氢气质量相等,根据反应方程式可知铁消耗得少、锌消耗得多,故C错误;
D、0﹣t2时段产生的氢气相等,氢元素全部来自稀盐酸,依据质量守恒定律可知,锌、铁消耗的盐酸质量相同,故D正确.
故选:C.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
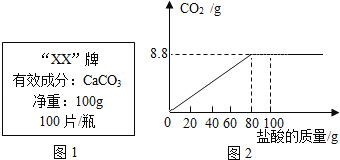
【题目】钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图1所示.现将125g盐酸分成5等份,逐次加到用50片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象如下.请根据有关信息回答问题.
第1次 | 第3次 | 第4次 | |
加入盐酸的质量(g) | 25 | 25 | 25 |
剩余固体的质量(g) | 45 | a | 30 |
(1)该品牌补钙药剂中CaCO3的质量分数是 ,a的数值为 .
(2)求该盐酸中溶质的质量分数(写出计算过程,计算结果保留一位小数).
(3)求恰好完全反应时所得溶液的溶质质量分数(写出计算过程,计算结果保留一位小数).