题目内容
【题目】根据如图回答问题。
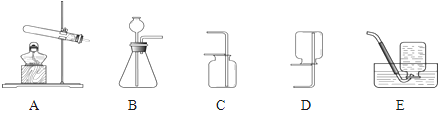
(1)高锰酸钾制取氧气选用的发生装置为_____(填序号,下同),收集装置为_____或E。写出该反应的符号表达式_____。若用装置E收集氧气,收集满应先_____后_____。
(2)实验室用过氧化氢制氧气选用的发生装置为_____,写出该反应的符号表达式_____。 该反应属于基本反应类型中的_____反应。
【答案】A C 2KMnO4![]() K2MnO4+MnO2+O2↑ 移出导管 熄灭酒精灯 B 2H2O2
K2MnO4+MnO2+O2↑ 移出导管 熄灭酒精灯 B 2H2O2![]() 2H2O+O2↑ 分解
2H2O+O2↑ 分解
【解析】
(1)如果用高锰酸钾制氧气就需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;故答案为:A;C;2KMnO4![]() K2MnO4+MnO2+O2↑;移出导管;熄灭酒精灯;
K2MnO4+MnO2+O2↑;移出导管;熄灭酒精灯;
(2)如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平,属于分解反应;故答案为:B;2H2O2![]() 2H2O+O2↑;分解;
2H2O+O2↑;分解;

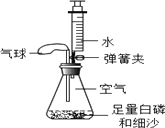
【题目】某研究小组用下图所示装置,探究能否用镁条代替红磷测定空气中氧气含量。
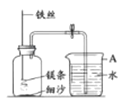
实验前,小组成员提出了不同的猜想。
【猜想与假设】
猜想1:可以代替,因为镁条与氧气反应后不会产生气体
猜想2:不能代替,查阅资料知金属镁很活泼,可能会与空气中的氮气反应
【进行实验】
步骤 | 实验操作 | 实验现象 |
Ⅰ | 组装好装置后,打开止水夹,手捂集气瓶,一段时间后,松开手 | 烧杯中导管口有气泡冒出,松手后,烧杯中导管末端有一段液柱 |
Ⅱ | 关闭止水夹,点燃镁条,迅速伸入集气瓶中,塞好塞子 | 镁条燃烧,放出大量热,发出耀眼白光,生成大量白烟,剩余固体为白色带状物 |
Ⅲ | 冷却至室温,打开止水夹 | 烧杯中水从导管进入集气瓶中,体积约为集气瓶体积的2/5 |
【解释与结论】
(1)Mg与氧气反应的化学方程式为_________。
(2)步骤Ⅰ说明装置的气密性_________。
(3)步骤Ⅱ中,关闭止水夹的目的是_________。
(4)推测猜想2成立的现象证据是_________。
【反思与评价】
(5)该小组认为,即使步骤Ⅲ中水的体积恰好占集气瓶体积的1/5,也不能说明猜想1成立,理由是_________。
(6)小组中同学对镁条与瓶中气体的反应提出了进一步的猜想:甲同学认为镁条先与O2反应,乙同学认为镁条先与N2反应。为进一步检验他们的猜想,可以进行的实验操作是:取少量镁条,点燃后迅速放入盛有空气的集气瓶中,待镁条熄灭后,________。