题目内容
【题目】某化学小组的同学对过量炭粉与氧化铁反应产物中气体成分进行探究。
(提出猜想)猜想Ⅰ:气体全部为CO;
猜想Ⅱ:气体全部为_________;
猜想Ⅲ:气体除CO外,还含有__________。
(查阅资料)CO气体能使湿润的氯化钯试纸变蓝色。
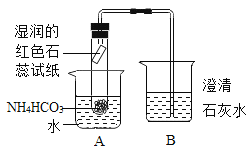
(实验方案)小组的同学设计了下图所示的装置并进行探究。
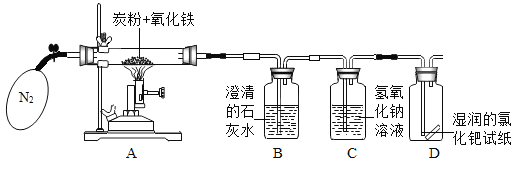
(问题讨论)
(1)实验开始前应先通入N2的作用是______________。
(2)若B中澄清石灰水变浑浊,则猜想_______不正确。B中发生反应的化学方程式为_______。
(3)实验证明猜想Ⅲ是正确的,则D中出现的现象是_______________。
(4)写出A中可能生成一氧化碳气体的1道化学方程式______________。
(5)从环保角度,你认为该实验还要在装置D导管末端__________________。
【答案】CO2 CO2 排尽装置内空气,以免造成干扰 Ⅰ Ca(OH)2+ CO2=CaCO3↓+H2O 湿润的氯化钯试纸变蓝色  (或
(或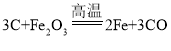 ) 将尾气进行燃烧处理(或收集)
) 将尾气进行燃烧处理(或收集)
【解析】
[提出猜想]:碳还原氧化铁能生成铁和碳的氧化物。则此氧化物可能是一氧化碳可能是二氧化碳。若为二氧化碳,则玻璃管中多余的木炭还会和二氧化碳反应生成一氧化碳。则生成的气体可能是一氧化碳、二氧化碳、一氧化碳和二氧化碳。故答案为:CO2、CO2;
(1)实验开始前,先通入氮气的目的是为了将装置内的空气排尽,防止加热时,产生其他杂质,干扰实验。故答案为:排尽装置内空气,以免造成干扰;
(2)B中澄清的石灰水变浑浊,则证明有二氧化碳气体生成。则猜想Ⅰ错误。澄清石灰水是氢氧化钙的水溶液,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水。故答案为:Ⅰ、Ca(OH)2+ CO2=CaCO3↓+H2O;
(3)猜想Ⅲ为气体是一氧化碳和二氧化碳。则除了能观察到B中澄清石灰水变浑浊证明有二氧化碳生成外,还应该在装置D中观察到湿润的氯化钯试纸变蓝色,则证明有一氧化碳那生成。故答案为:湿润的氯化钯试纸变蓝色;
(4)根据猜想可知,装置A中的一氧化碳可能来自与碳还原氧化铁,生成铁和一氧化碳。或者是碳还原氧化铁生成了二氧化碳,二氧化碳和碳在高温下反应生成一氧化碳。故答案为: (或
(或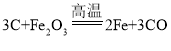 );
);
(5)由于生成的一氧化碳有毒,且属于大气污染物,则应该增添一个尾气处理装置。故答案为:将尾气进行燃烧处理(或收集)。

 阅读快车系列答案
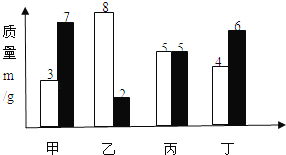
阅读快车系列答案【题目】在一定条件下,甲、乙、丙、丁四种物质在一密闭容器中充分反应,测得反应前后各物质的质量如表所示。根据表中信息判断下列说法正确的是
物 质 | 甲 | 乙 | 丙 | 丁 |
反应前的质量 | 2 | 30 | 20 | 10 |
反应后的质量 | m | 39 | 5 | 16 |
A.该反应是化合反应B.甲一定是该反应的催化剂
C.反应过程中乙、丙变化的质量比为3:5D.丙可能是单质
【题目】材料在交通工具上有着广泛的应用,根据下列信息回答问题。
应用 |
| 大飞机 C919 |
共享汽车 |
用到的材料 | 轮胎:橡胶 | 机翼:铝锂合金 | 车身:钢 |
(1)上述交通工具用到的材料属于金属材料的是__________ (填一种即可),属于有机合成材料的是__________。
(2)汽车车身表面的烤漆不仅美观,还能起到防锈的作用,工业上常用稀盐酸来除铁锈(Fe2O3),该反应的化学方程式是______________。
(3)化石燃料的大量使用,带来了环境的污染和资源的枯竭等问题,共享汽车在广泛推广使用乙醇汽油,其好处是___________。