题目内容
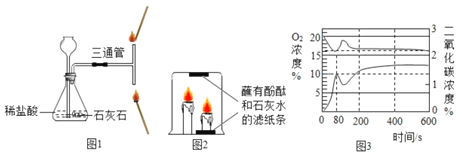
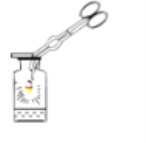
【题目】下图是铁丝在氧气中燃烧的装置,请回答下列问题:
(1)观察到的实验现象是______________________________,反应的化学方程式为 __________________。
(2)铁丝能在氧气中燃烧,却很难在空气中燃烧,这说明了_______________________ 。
(3)小明同学点燃系在光亮螺旋状细铁丝底端的火柴后,立即插入盛满氧气的集气瓶中,细铁丝没有燃烧,原因是________________________________ 。
【答案】剧烈燃烧,火星四射,放出热量,产生黑色固体 3Fe+2O2![]() Fe3O4 氧气浓度越大,可燃物越易燃烧 火柴燃烧消耗了瓶中的氧气,使铁丝没有足够的氧气燃烧
Fe3O4 氧气浓度越大,可燃物越易燃烧 火柴燃烧消耗了瓶中的氧气,使铁丝没有足够的氧气燃烧
【解析】
(1)铁丝在氧气中燃烧的现象是剧烈燃烧,火星四射,放出热量,产生黑色固体,故填剧烈燃烧,火星四射,放出热量,产生黑色固体;
铁和氧气在点燃的条件下反应生成四氧化三铁,故反应的化学方程式写为:3Fe+2O2![]() Fe3O4。
Fe3O4。
(2)铁丝能在氧气中燃烧,却很难在空气中燃烧,原因是氧气浓度越大,可燃物越易燃烧,故填氧气浓度越大,可燃物越易燃烧。
(3)小明同学点燃系在光亮螺旋状细铁丝底端的火柴后,立即插入盛满氧气的集气瓶中,细铁丝没有燃烧是因为将铁丝伸到氧气中过快,火柴燃烧消耗了瓶中的氧气,使铁丝没有足够的氧气燃烧,故填火柴燃烧消耗了瓶中的氧气,使铁丝没有足够的氧气燃烧。

【题目】某化学兴趣小组为了測定粗锌中锌的质量分数,在10g粗锌中分5次共加入50.0g稀硫酸(杂质不与硫酸反应),部分数据如下表。
容器中硫酸的质量/g | 10 | 20 | 40 | 50 |
气体质量/g | 0.1 | 0.2 | m | 0.3 |
根据实验数据回答下列问题:
(1)当硫酸滴入40g时,对应的气体质量m是_______g。
(2)粗锌中锌的质量分数是多少?__________________