题目内容
【题目】钠及其化合物是中学化学学习和研究的重要内容.

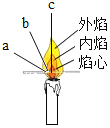
(1)如图1是钠的原子结构示意图,钠在反应中失电子后形成离子的符号是_____.
(2)钠在氯气中燃烧生成氯化钠,化学方程式为_____.
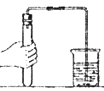
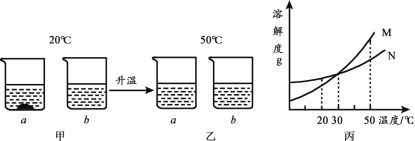
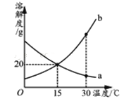
(3)配制一瓶符合如图2所示的氯化钠溶液,需氯化钠_____g;小明同学配制的氯化钠溶液质量分数偏小了,请写出他操作中可能出现的错误(提示:1g以下用游码,至少答出两点)_____.
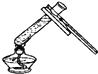
(4)如何测定一瓶苏打水的酸碱度(写出实验操作步骤)_____.
(5)小苏打受热分解生成碳酸钠、二氧化碳和水,化学方程式为_____.
(6)钛和钛合金性能优良,广泛用于航空、造船和化学工作中.工业上常用钠来制取钛,在高温时,钠与四氯化钛(TiCl4)反应生成氯化钠和钛.若用该方法制取2.4kg钛,理论上需要钠的质量是多少_____?
【答案】Na+ 2Na+Cl2![]() 2NaCl 4.5 称量时砝码和试剂放反了,量取水时仰视读数,溶解前用蒸馏水润洗了烧杯 用干燥的玻璃棒蘸取(或胶头滴管吸取)少量的待测溶液,并滴在放在干燥的玻璃皿或白瓷板上的干燥pH试纸上,再把试纸显示的颜色与标准比色卡比较,即可得出待测溶液的Ph 2NaHCO3
2NaCl 4.5 称量时砝码和试剂放反了,量取水时仰视读数,溶解前用蒸馏水润洗了烧杯 用干燥的玻璃棒蘸取(或胶头滴管吸取)少量的待测溶液,并滴在放在干燥的玻璃皿或白瓷板上的干燥pH试纸上,再把试纸显示的颜色与标准比色卡比较,即可得出待测溶液的Ph 2NaHCO3![]() Na2CO3+H2O+CO2↑ 4.6kg
Na2CO3+H2O+CO2↑ 4.6kg
【解析】
(1)根据钠原子的结构图进行分析;
(2)根据钠和氯气会生成氯化钠进行分析.
(3)根据溶质质量=溶液质量×溶质质量分数进行分析;根据俯视读数会使读出的数据大于实际数据进行分析;
(4)根据测定溶液pH的方法判断,使用pH试纸测定溶液pH,测定时,用玻璃棒蘸取待测溶液,滴在试纸上,然后再与标准比色卡对照,便可测出溶液的pH;
(5)根据碳酸氢钠受热后的产物进行分析,
(6)根据在高温时,钠与四氯化钛(TiCl4)反应生成氯化钠和钛,然后结合题中的数据进行解答.
(1)钠元素的最外层有1个电子,容易失去电子,形成钠离子Na+;
(2)钠和氯气在点燃的条件下生成氯化钠,故答案为:2Na+Cl2![]() 2NaCl;
2NaCl;
(3)氯化钠的质量为:500mL×1g/mL×0.9%=4.5g,小明同学配制的氯化钠溶液质量分数偏小了,可能是称量时砝码和试剂放反了,量取水时仰视读数,溶解前用蒸馏水润洗了烧杯;
(4)测定溶液酸碱度的方法:用干燥的玻璃棒蘸取(或胶头滴管吸取)少量的待测溶液,并滴在放在干燥的玻璃皿或白瓷板上的干燥pH试纸上,再把试纸显示的颜色与标准比色卡比较,即可得出待测溶液的pH;
(5)碳酸氢钠在加热的条件下生成碳酸钠、水和二氧化碳,化学方程式为:
2NaHCO3![]() Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;
(6)设理论上需要钠的质量是x,则
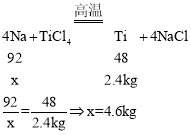
所以制取2.4kg钛,理论上需要钠的质量是4.6kg。

【题目】小明同学对所学部分化学知识归纳如下,其中正确的是
A | 须辨清的物质 | B | 初中化学中常见的“三” |
干冰不是冰——而是固体CO2 纯碱不是碱——而是盐 水银不是银——而是汞 | 三种可燃性气体——CO、H2、N2 三种有毒物质——CO、亚硝酸钠、H2 三种基本粒子——原子、分子、离子 | ||
C | 化学巨匠及其杰出贡献 | D | 符号中数字“2”的意义 |
张青莲——测量相对原子质量 拉瓦锡——测定空气的组成 侯德榜——发明联合制碱法 | 2O:两个氧分子
O2:两个氧原子 |
A.AB.BC.CD.D