题目内容
【题目】金属钨(W)可作白炽灯泡的灯丝。工业上用黑钨矿[主要含有FeWO4(钨酸亚铁)]制得金属钨(W)的工艺流程如图所示

(1)金属钨可用作灯丝,是因为钨的_____ 高;H2WO4中钨的化合价为_____。
(2)反应①的化学方程式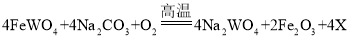 ,X的化学式为_____ ;反应③属于_____ 反应(填基本反应类型)。
,X的化学式为_____ ;反应③属于_____ 反应(填基本反应类型)。
(3)反应④的化学方程式为_____ 该反应中氢气表现出的性质是_____。
【答案】熔点 +6价 CO2 分解 3H2+WO3![]() 3H2O+W 还原性
3H2O+W 还原性
【解析】
(1)金属钨可用作灯丝,是因为钨的熔点高;H2WO4中氢元素为+1价,氧元素为-2价,设钨的化合价为x,根据化合物中正负化合价的代数和为零可得,(+1)×2+x+(-2)×4=0,x=+6,钨的化合价为+6价。
(2)反应①的化学方程式为4FeWO4+4Na2CO3+O2=4Na2WO4+2Fe2O3+4X,反应前Fe为4,W为4,O为30,Na为8,C为4,反应后现有Fe为4,W为4,O为22,Na为8,C为0,少 O为8,C为4,包含在4个X分子中,所以每个X分子含有一个碳原子和两个氧原子,所以X的化学式为 CO2;
反应③是H2WO4![]() H2O+WO3,为一变多,符合分解反应的特征,属于分解反应。
H2O+WO3,为一变多,符合分解反应的特征,属于分解反应。
(3)反应④是氢气和氧化钨反应生成水和钨,对应的化学方程式为 3H2+WO3![]() 3H2O+W,该反应中氢气得氧为还原剂,体现还原性。
3H2O+W,该反应中氢气得氧为还原剂,体现还原性。
故答案为:
(1)熔点;+6价。
(2)CO2;分解。
(3)3H2+WO3![]() 3H2O+W;还原性。
3H2O+W;还原性。

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案
相关题目