题目内容
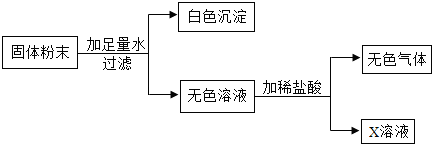
一包白色粉末可能由碳酸钠、硫酸钠和氯化钠中的2种或3种组成.经实验得知其中肯定含有碳酸钠和硫酸钠.为了确定是否含有氯化钠,某同学设计了以下实验.请该同学的思路填写下表:| 实验操作步骤 | 实验目的、现象及结论 |
| (1)取少量白色固体粉末,配成水溶液,向其中加入足量的稀酸A,A为___________ | 除去____________________ |
| (2)继续加入足量的B,B为___________ | 除去硫酸钠 |
| (3)向(2)中的滤液中加入C,C为__________溶液 | 若有_________,证明原白色固体粉末中肯定含有氯化钠;否则不含氯化钠 |
【答案】分析:检验混合物中是否含有氯化钠也就检验是否含有氯离子,检验氯离子用硝酸银和稀硝酸.为排除碳酸根离子和硫酸根离子的干扰,我们可以先用稀硝酸来排除碳酸根离子,用硝酸钡来排除硫酸根离子的干扰.
解答:解:白色粉末中一定含有碳酸钠和硫酸钠,要想证明一定含有氯化钠,只需证明一定含有氯离子就可以了.检验氯离子用硝酸银和稀硝酸.但我们要先排除碳酸根离子的干扰,所以我们先加稀硝酸除碳酸根离子,加硝酸钡除硫酸根离子.
故答案为:
点评:在检验氯离子时,一定先排除碳酸根离子和硫酸根离子的干扰,否则也能得到白色沉淀,但沉淀不一定是硝酸银.
解答:解:白色粉末中一定含有碳酸钠和硫酸钠,要想证明一定含有氯化钠,只需证明一定含有氯离子就可以了.检验氯离子用硝酸银和稀硝酸.但我们要先排除碳酸根离子的干扰,所以我们先加稀硝酸除碳酸根离子,加硝酸钡除硫酸根离子.
故答案为:
| 实验操作步骤 | 实验目的、现象及结论 |
| (1)取少量白色固体粉末,配成水溶液,向其中加入足量的稀酸A,A为【HNO3(或H2SO4)】 | 除去【Na2CO3】 |
| (2)继续加入足量的B,B为【Ba(NO3)2】 | 除去硫酸钠 |
| (3)向(2)中的滤液中加入C,C为【AgNO3】溶液 | 若有【白色沉淀】,证明原白色固体粉末中肯定含有氯化钠;否则不含氯化钠 |
点评:在检验氯离子时,一定先排除碳酸根离子和硫酸根离子的干扰,否则也能得到白色沉淀,但沉淀不一定是硝酸银.

练习册系列答案
相关题目