题目内容
(2012?乐陵市二模)学习碳酸钠知识时,老师做碳酸钠溶液和澄清石灰水反应演示实验,并对悬浊液过滤,得到澄清滤液.课堂上老师的提问和同学们的回答如图所示:
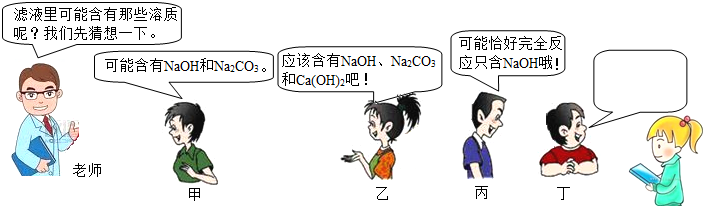
(1)你认为甲、乙、丙同学的猜想都合理吗?如有不合理的请说明理由;
(2)假设你是丁同学,请你也提出一个与甲、乙、丙同学不同的猜想,把猜想写在
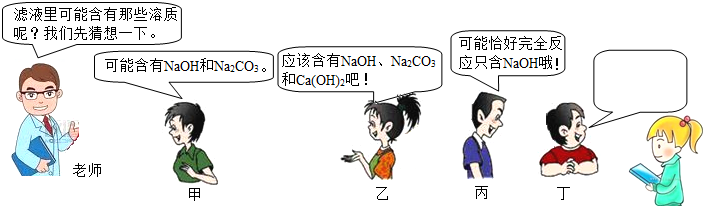
(1)你认为甲、乙、丙同学的猜想都合理吗?如有不合理的请说明理由;
乙同学的猜想不合理,因为Na2CO3与Ca(OH)2会发生反应,不可能共存
乙同学的猜想不合理,因为Na2CO3与Ca(OH)2会发生反应,不可能共存
.(2)假设你是丁同学,请你也提出一个与甲、乙、丙同学不同的猜想,把猜想写在
可能含有NaOH和Ca(OH)2
可能含有NaOH和Ca(OH)2
中.并对你自己的猜想设计一个简单的实验加以证明.| 实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |
| 取样于试管中, 通入二氧化碳(或加入碳酸钠溶液) 通入二氧化碳(或加入碳酸钠溶液) |
试管内出现白色浑浊 试管内出现白色浑浊 |
自己的猜想成立 |
分析:根据题干提供信息进行分析:碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应时可能未恰好完全反应,故氢氧化钙或碳酸钠都有可能剩余;但是两种反应物不会同时剩余;检验氢氧化钙的存在可用二氧化碳或可溶性碳酸盐溶液.
解答:解:(1)物质间发生化学反应时存在一定量的关系,如果某种反应物过量,会有剩余,但是两种反应物不会同时剩余;
故答案为:乙同学的猜想不合理.因为Na2CO3与Ca(OH)2会发生反应,不可能共存;
(2)根据化学反应:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,可以知道,反应后滤液中一定有氢氧化钠存在,若碳酸钠过量,则含有碳酸钠,即甲同学的猜想;若恰好完全反应,则只含有氢氧化钠,即丙同学的猜想;若氢氧化钙过量,则含有氢氧化钙,即丁同学可能提出的猜想;
要证明丁同学的猜想,就是证明含有氢氧化钙,可以依据氢氧化钙的性质进行判断,向溶液中通入二氧化碳或与可溶性碳酸盐反应生成沉淀来确定;
故答案为:可能含有NaOH和Ca(OH)2;
故答案为:乙同学的猜想不合理.因为Na2CO3与Ca(OH)2会发生反应,不可能共存;
(2)根据化学反应:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,可以知道,反应后滤液中一定有氢氧化钠存在,若碳酸钠过量,则含有碳酸钠,即甲同学的猜想;若恰好完全反应,则只含有氢氧化钠,即丙同学的猜想;若氢氧化钙过量,则含有氢氧化钙,即丁同学可能提出的猜想;
要证明丁同学的猜想,就是证明含有氢氧化钙,可以依据氢氧化钙的性质进行判断,向溶液中通入二氧化碳或与可溶性碳酸盐反应生成沉淀来确定;
故答案为:可能含有NaOH和Ca(OH)2;
| 实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |
| 取样于试管中,通入二氧化碳(或加入碳酸钠溶液) | 试管内出现白色浑浊 | 自己的猜想成立 |
点评:物质间发生化学反应时存在一定量的关系,若某种反应物过量,会有剩余,但不会反应物同时剩余;在判断物质组成成分时,可以依据物质的性质设计实验进行推断.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
 (2012?乐陵市二模)为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如下表:
(2012?乐陵市二模)为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如下表: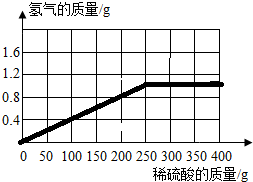
 (2012?乐陵市二模)已知砷和铟的原子结构示意图如下:
(2012?乐陵市二模)已知砷和铟的原子结构示意图如下: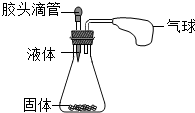 (2012?乐陵市二模)如图所示,挤压胶头滴管中的液体,使之与瓶中固体接触,可使小气球鼓起来.请写出符合下列要求的化学方程式:
(2012?乐陵市二模)如图所示,挤压胶头滴管中的液体,使之与瓶中固体接触,可使小气球鼓起来.请写出符合下列要求的化学方程式: