题目内容
某同学对下列4个实验都设计了两种方案,其中方案一、方案二都合理的是
| 选项 | A | B | C | D |
| 实验目的 | 除去炭粉中少量的氧化铜 | 证明长期露置的氢氧化钠溶液已变质 | 鉴别硫酸钾和硝酸铵 | 证明稀醋酸溶液呈酸性 |
| 方案一 | 加稀硫酸 | 加足量稀盐酸 | 看外观 | 加无色酚酞试液 |
| 方案二 | 高温灼烧 | 加澄清石灰水 | 加熟石灰研磨闻气味 | 加氢氧化钠溶液 |
B
试题分析:A、在高温下灼烧,炭粉会与空气中氧气反应生成二氧化碳气体,而氧化铜不反应,故方案二不合理;
B、证明氢氧化钠是否变质,主要是检验是否存在碳酸钠;方案一、加稀盐酸NaOH+HCl=NaCl+H2O 无明显现象,Na2CO3+2HCl=2NaCl+H2O+CO2↑,产生气泡,根据产生气泡,就证明含有碳酸钠,样品已变质,反之就没有变质,故合理;方案二:加澄清的石灰水 Ca(OH)2、NaOH二者不反应,无明显现象,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH,产生白色沉淀,根据产生沉淀,就证明含有碳酸钠,样品已变质.反之就没有变质,故合理;综上所述,故B正确;
C、方案一:看外观 硫酸钾和硝酸铵二者都是白色固体,故不合理;
D、方案一:用无色的酚酞试液不能证明稀醋酸溶液呈酸性,因为酚酞试液遇到酸性和中性溶液都不变色,故不合理;方案二:醋酸与氢氧化钠反应生成醋酸钠、水,无现象,故不合理;综上所述,故D错误;
故选B。
点评:在具体实验设计中要对其原理要透彻理解,可根据物质的物理性质和化学性质结合实验的目的进行分析判断。

练习册系列答案
相关题目



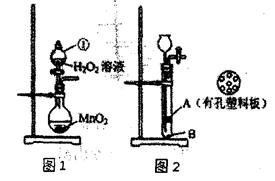
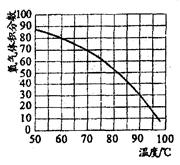

 CaCO3+CO2↑
CaCO3+CO2↑