题目内容
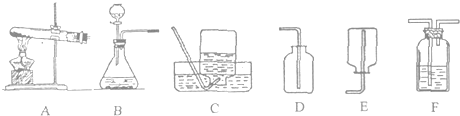
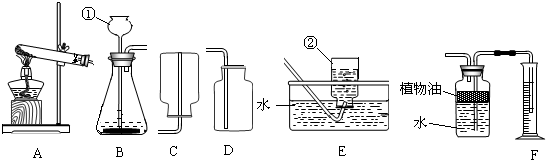
实验室常用如图所示装置制取气体,请你根据所学知识回答下列问题.

(1)若选用a高锰酸钾(K2MnO4)在加热的条件制取氧气,则选用的发生装置为
(2)写出选用B制取氧气的文字表达式或化学方程式
(3)有一名同学欲用F装置排空气法收集氧气,则氧气应从导管口
(5)小文查阅相关资料知:锌(Zn)和稀H2SO4能在常温常压下反应,生成硫酸锌(ZnSO4)和氢气(H2),且氢气难溶于水,密度是已知发现的气体中最小的.试问实验室制取H2可选用的发生装置为

(1)若选用a高锰酸钾(K2MnO4)在加热的条件制取氧气,则选用的发生装置为
B
B
,若选用b过氧化氢(H2O2)在二氧化锰(MnO2)作为催化剂的条件下制取氧气,发生装置为A
A
,反应原理为2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
;如从节能角度分析应
| ||
b
b
(填a或b).(2)写出选用B制取氧气的文字表达式或化学方程式
高锰酸钾
锰酸钾+二氧化锰+氧气或2KMnO4
K2MnO4+MnO2+O2↑
| 加热 |
| ||
高锰酸钾
锰酸钾+二氧化锰+氧气或2KMnO4
K2MnO4+MnO2+O2↑
| 加热 |
| ||
(3)有一名同学欲用F装置排空气法收集氧气,则氧气应从导管口
b
b
通入,验证此装置是否收集满氧气的方法为将带火星的木条放于c处,若木条复燃则收集满了
将带火星的木条放于c处,若木条复燃则收集满了
(5)小文查阅相关资料知:锌(Zn)和稀H2SO4能在常温常压下反应,生成硫酸锌(ZnSO4)和氢气(H2),且氢气难溶于水,密度是已知发现的气体中最小的.试问实验室制取H2可选用的发生装置为
A
A
(填序号),收集装置为C
C
(原因是氢气难溶于水
氢气难溶于水
)或E
E
(原因是氢气的密度是气体中最小的
氢气的密度是气体中最小的
).其反应原理为:Zn+H2SO4=ZnSO4+H2↑
Zn+H2SO4=ZnSO4+H2↑
.分析:(1)加热高锰酸钾属于固体加热型,故选发生装置B,过氧化氢(H2O2)在二氧化锰(MnO2)作为催化剂的条件下制取氧气属于固液常温型,故选发生装置A,并据反应原理书写方程式,可知过氧化氢分解制取氧气不需加热,可节约能源;
(2)B装置是用加热高锰酸钾的方法制取氧气,据此分析解答;
(3)氧气的密度比空气大,据此确定进气口,验证氧气是否收集满的方法是将带火星的木条放于出气口,观察木条是否复燃进行判断;
(4)据反应物状态和反应条件选择发生装置,据气体的密度和溶解性选择收集装置,并据反应原理分析解答.
(2)B装置是用加热高锰酸钾的方法制取氧气,据此分析解答;
(3)氧气的密度比空气大,据此确定进气口,验证氧气是否收集满的方法是将带火星的木条放于出气口,观察木条是否复燃进行判断;
(4)据反应物状态和反应条件选择发生装置,据气体的密度和溶解性选择收集装置,并据反应原理分析解答.
解答:解:(1)加热高锰酸钾属于固体加热型,故选发生装置B,过氧化氢(H2O2)在二氧化锰(MnO2)作为催化剂的条件下制取氧气属于固液常温型,故选发生装置A,反应原理为:2H2O2
2H2O+O2↑,用过氧化氢制取氧气,不需要加热,可节约能源;
(2)B装置是用加热高锰酸钾的方法制取氧气,加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应原理是:高锰酸钾
锰酸钾+二氧化锰+氧气或2KMnO4
K2MnO4+MnO2+O2↑;
(3)氧气的密度比空气大,欲用F装置排空气法收集氧气,则氧气应从导管口b通入,将空气挤压到集气瓶上部排出;验证氧气是否收集满的方法是将带火星的木条放于出气口c处,观察木条是否复燃进行判断;
(4)锌(Zn)和稀H2SO4能在常温常压下反应,生成硫酸锌(ZnSO4)和氢气(H2),属于固液常温型,故选发生装置A,氢气难溶于水,密度是已知发现的气体中最小的,所以可用排水法或向下排空气法收集;其反应原理为:Zn+H2SO4=ZnSO4+H2↑;
故答为:(1)B;A;2H2O2
2H2O+O2↑;b;
(2)高锰酸钾
锰酸钾+二氧化锰+氧气或2KMnO4
K2MnO4+MnO2+O2↑;
(3)b;将带火星的木条放于c处,若木条复燃则收集满了;
(4)A;C;氢气难溶于水;E;氢气的密度是气体中最小的;Zn+H2SO4=ZnSO4+H2↑.
| ||
(2)B装置是用加热高锰酸钾的方法制取氧气,加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应原理是:高锰酸钾
| 加热 |
| ||
(3)氧气的密度比空气大,欲用F装置排空气法收集氧气,则氧气应从导管口b通入,将空气挤压到集气瓶上部排出;验证氧气是否收集满的方法是将带火星的木条放于出气口c处,观察木条是否复燃进行判断;
(4)锌(Zn)和稀H2SO4能在常温常压下反应,生成硫酸锌(ZnSO4)和氢气(H2),属于固液常温型,故选发生装置A,氢气难溶于水,密度是已知发现的气体中最小的,所以可用排水法或向下排空气法收集;其反应原理为:Zn+H2SO4=ZnSO4+H2↑;
故答为:(1)B;A;2H2O2
| ||
(2)高锰酸钾
| 加热 |
| ||
(3)b;将带火星的木条放于c处,若木条复燃则收集满了;
(4)A;C;氢气难溶于水;E;氢气的密度是气体中最小的;Zn+H2SO4=ZnSO4+H2↑.
点评:学会比较用高锰酸钾和用过氧化氢溶液和二氧化锰制取氧气的区别;掌握制取氧气和氢气的反应原理、制法及验满等,并结合题意灵活分析解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
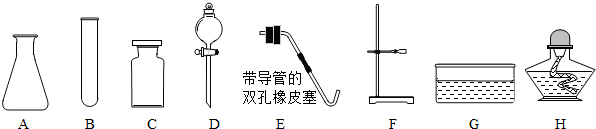
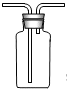
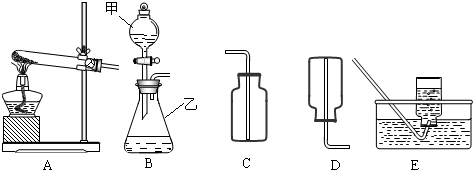
 通过化学课程的学习,我们收获很多.
通过化学课程的学习,我们收获很多.