题目内容
在加入Na2CO3溶液的过程中,开始时没有发现沉淀生成,说明废液中的溶质除含有CaCl2外,还含有_________。
(2)计算Na2CO3溶液中溶质的质量分数(计算结果精确到0.1%)。
【解析】石灰石与稀盐酸反应后的废液中一定有CaCl2,此外还可能含有反应中过量的稀盐酸,分析坐标图可知,当加入5 g碳酸钠溶液时没有产生沉淀,由此可知废液中除含有CaCl2外,还一定含有盐酸,开始加入的5 g碳酸钠溶液先与废液中剩余的盐酸发生反应,故没有沉淀出现。再由坐标图的拐点知,向废液中加入25 g碳酸钠溶液时产生了5 g沉淀,即与废液中的氯化钙反应的Na2CO3溶液的质量为25 g-5 g=20 g,同时生成5 g碳酸钙沉淀,以此为突破口,根据化学方程式进行计算即可。 答案:(1)HCl
(2)解:由图像可知,有25 g-5 g=20 g Na2CO3溶液与氯化钙溶液发生反应,生成5 g碳酸钙沉淀。
设20 g Na2CO3溶液中溶质的质量为x。
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 100
x 5 g
106/100=x/5 g x=5.3 g
该Na2CO3溶液中溶质的质量分数为:5.3 g/20 g×100%=26.5%
答:Na2CO3溶液中溶质的质量分数为26.5%。
【易错点点睛】解答坐标图像题的突破口一般为曲线上的两个点,即起点和拐点(或终点),准确分析并理解两点对应的纵、横坐标数据的意义是解题的关键,找出解题所需数据后,按照化学方程式计算![]() 或溶液中溶质质量分数计算的方法进行解答即可。
或溶液中溶质质量分数计算的方法进行解答即可。

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
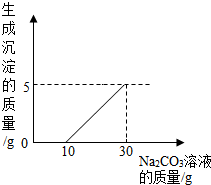 刘明用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该废液,测定Na2CO3溶液中溶质的质量分数.他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如下图所示.
刘明用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该废液,测定Na2CO3溶液中溶质的质量分数.他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如下图所示.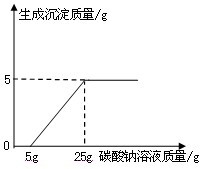 某化学兴趣小组在用石灰石(杂质不与酸反应,也不溶于水)或稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他们决定利用该废液测定这瓶Na2CO3溶液的溶质质量分数.他们先将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如右图所示.
某化学兴趣小组在用石灰石(杂质不与酸反应,也不溶于水)或稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他们决定利用该废液测定这瓶Na2CO3溶液的溶质质量分数.他们先将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如右图所示.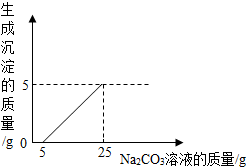 刘明用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该废液,测定Na2CO3溶液中溶质的质量分数.他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示.
刘明用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该废液,测定Na2CO3溶液中溶质的质量分数.他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示. 刘明用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该废液测定Na2CO3溶液中溶质的质量分数.他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示.
刘明用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该废液测定Na2CO3溶液中溶质的质量分数.他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示.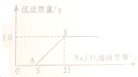 小华用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取CO2.实验完毕,他的同伴小阳决定用实验后的废液,测定桌上另一瓶Na2CO3溶液的溶质质量分数.小阳将废液过滤后,向滤液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示.
小华用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取CO2.实验完毕,他的同伴小阳决定用实验后的废液,测定桌上另一瓶Na2CO3溶液的溶质质量分数.小阳将废液过滤后,向滤液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示.