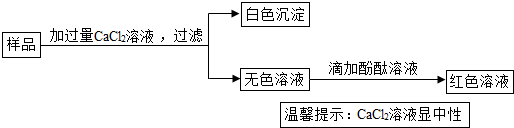
��Ŀ����
 ʵ������һƿ���õ�NaOH����ȡ13.3g ��NaOH��Ʒ������ΪNa2CO3�����ձ��У�Ȼ�����ձ�����μ�����������19.6%��ϡ���ᣬ��Ӧ�����ͼ��ʾ��
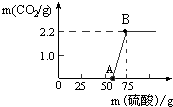
ʵ������һƿ���õ�NaOH����ȡ13.3g ��NaOH��Ʒ������ΪNa2CO3�����ձ��У�Ȼ�����ձ�����μ�����������19.6%��ϡ���ᣬ��Ӧ�����ͼ��ʾ����1���Լ��㣺
�ٸ���Ʒ��Na2CO3������Ϊ���٣�
��B������Ӧ����Һ�����ʵ���������Ϊ���٣�
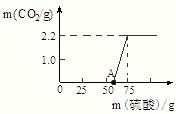
��2����ͼ��0��A��˵������NaOH ��Na2CO3�Ļ����Һ�У�����ǿ�ᣬ���ȷ�Ӧ��������
��������1������ͼ������ж�ǡ����ȫ��Ӧʱ���ɶ�����̼����2.2g��Ȼ����뻯ѧ��Ӧ����ʽ������̼���Ƶ���������B������Ϊ�����ƣ������������غ������Һ���������ټ������ʵ�����������
��2����ǿ��ʱ����ͼ����Կ���25g�������ʱû���������ɣ����ȷ��������кͷ�Ӧ��������ԭ���غ��֪��ԭ�����е��Ƶ��������������е��ƣ�����������ȣ�
��2����ǿ��ʱ����ͼ����Կ���25g�������ʱû���������ɣ����ȷ��������кͷ�Ӧ��������ԭ���غ��֪��ԭ�����е��Ƶ��������������е��ƣ�����������ȣ�
����⣺��1������̼���Ƶ�����Ϊx����
Na2CO3+H2SO4�TNa2SO4+CO2��+H2O
106 44
x 2.2g
=
���x=5.3g����̼���Ƶ�����Ϊ5.3g��
��B��ʱΪ��������Һ�������������Ƶ�����Ϊy��
��������������غ��H2SO4��Na2SO4��
98 142
75��19.6% y
=
�����y=21.3g��
��Һ����Ϊ13.3g+75g-2.2g=86.1g
�����ʵ���������Ϊ
��100%=24.7%��
�����ʵ���������Ϊ24.7%��
��2����ͼ���֪����25g����ʱ���������ɣ������ĽǶȿ�֪25g��50g�ᷢ��̼���������ᷴӦ�����������ƣ�����ԭ���غ�ĽǶ���������Һ�е���������Ϊ�����ƣ���ԭ��Ʒ�е������������е�����ȣ�������������ȣ��ʴ�Ϊ��NaOH����ȣ�
Na2CO3+H2SO4�TNa2SO4+CO2��+H2O
106 44
x 2.2g
| 106 |
| x |
| 44 |
| 2.2g |
���x=5.3g����̼���Ƶ�����Ϊ5.3g��
��B��ʱΪ��������Һ�������������Ƶ�����Ϊy��
��������������غ��H2SO4��Na2SO4��
98 142
75��19.6% y
| 98 |
| 75��19.6% |
| 142 |
| y |
��Һ����Ϊ13.3g+75g-2.2g=86.1g
�����ʵ���������Ϊ
| 21.3g |
| 86.1g |
�����ʵ���������Ϊ24.7%��
��2����ͼ���֪����25g����ʱ���������ɣ������ĽǶȿ�֪25g��50g�ᷢ��̼���������ᷴӦ�����������ƣ�����ԭ���غ�ĽǶ���������Һ�е���������Ϊ�����ƣ���ԭ��Ʒ�е������������е�����ȣ�������������ȣ��ʴ�Ϊ��NaOH����ȣ�
���������⿼��ѧ������ͼ���뻯ѧ��Ӧ�ķ�����ѧ��Ӧ��ȷͼ���еĵ㡢������Ӧ�Ļ�ѧ��Ӧ����ȷԭ���غ㷽���ڽ����е�Ӧ�ã�

��ϰ��ϵ�д�
�����Ŀ
 ijУ�о���ѧϰС�������һ����Ȥ��ʵ��̽����
ijУ�о���ѧϰС�������һ����Ȥ��ʵ��̽����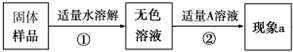 ʵ������һƿ���õ��������ƹ��壬ijͬѧ���˽����Ƿ���ʣ����������ʵ�飬������һ���������̽�����
ʵ������һƿ���õ��������ƹ��壬ijͬѧ���˽����Ƿ���ʣ����������ʵ�飬������һ���������̽�����