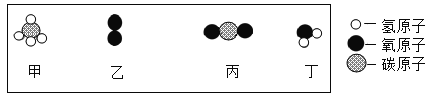
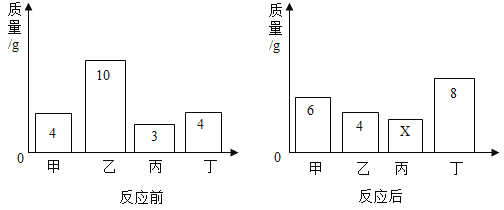
题目内容
【题目】请结合如图所示实验装置,回答下列问题。
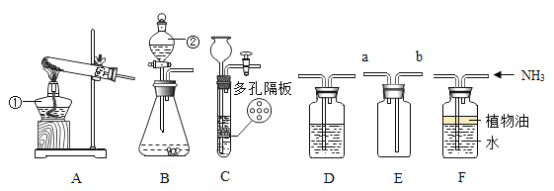
(1)写出①号仪器的名称:__________。
(2)用高锰酸钾制取氧气选用的发生装置是________(选填序号),反应的化学方程式为________________________。
(3)要获得干燥的O2,应先将气体通过盛有_____________(选填H2S04或NaOH溶液)的D装置,再用E装置收集,气体应从____ 端通入(选填“a”或“b”)。
(4)实验室可用B或C装置制CO2,反应的化学方程式为____________________,相对于B装置,C装置的优点有________________________。
(5)若用F装置收集NH3,油层的作用是________________________。
【答案】酒精灯 A ![]() H2SO4 b CaCO3+2HCl=CaCl2+H2O+CO2↑ 能使反应随时进行或停止 防止氨气溶于水
H2SO4 b CaCO3+2HCl=CaCl2+H2O+CO2↑ 能使反应随时进行或停止 防止氨气溶于水
【解析】
(1)①号仪器的名称是酒精灯。
(2)实验室用高锰酸钾制取氧气时,反应物的状态是固体,反应条件是加热,可选用的气体发生装置是A。高锰酸钾在加热的条件下可以分解产生二氧化锰、锰酸钾和氧气;化学方程式为: ![]() 。
。
(3)浓硫酸具有吸水性,而氢氧化钠溶液没有吸水性,所以应该用浓硫酸来进行干燥;氧气的密度比空气大,所以用E装置来收集氧气时,氧气从长管进入。
(4)实验室可用B或C装置制CO2,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,C相对于B装置的优点是能使反应随时进行或停止,其原理是:关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止;打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行。
(5)若用F装置收集NH3,油层的作用是防止氨气溶于水。

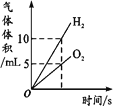
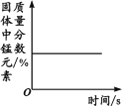
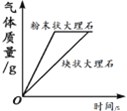
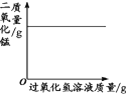
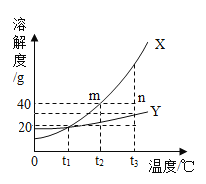
【题目】下列图像不能正确反映对应变化关系的是
|
|
|
|
A.将水通电电解一 段时间 | B.加热一定量的高 锰酸钾固体 | C.向两份相等质量的块状大理石和粉末状大理石中分别加入过量的等浓度的稀盐酸 | D.向一定量的二氧化锰中加入过氧化氢溶液 |
A. A B. B C. C D. D
【题目】在探究铝化学性质时发现铝与稀盐酸反应比与稀硫酸反应剧烈,化学兴趣小组进行了如下探究:
(1)铝与稀盐酸反应的化学方程式为_____。
(2)铝片使用前需要打磨的原因是_____,铝能被用来制作导线是因为其具有_____性。
(3)实验过程中,可以通过观察_____来比较铝与稀盐酸和稀硫酸反应的剧烈程度。
(4)(作出猜想)猜想一:Cl-对反应起了促进作用;
猜想二:SO![]() 对反应起了阻碍作用;
对反应起了阻碍作用;
猜想三:以上两种猜想同时成立。
(进行实验)
实验 | 实验操作 |
实验1 | 将铝片加入到10mLpH=1的稀盐酸中,然后向其中滴加CuSO4溶液 |
实验2 | 将铝片加入到10mLpH=1的稀硫酸中,然后向其中滴加浓盐酸 |
实验3 | 将铝片加入到10mLpH=1的稀盐酸中,然后向其中滴加Na2SO4溶液 |
(分析并得出结论)
①同学们认为实验1不可行,理由是_____。
②同学们认为实验2思路不正确,改进的方法是_____。
③实验3没有明显现象,证明猜想_____不成立。
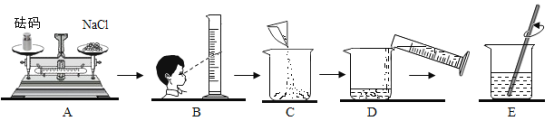
【题目】(7分)某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题。
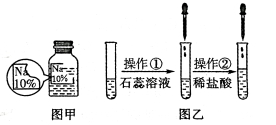
【猜想与假设】其溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种。
【资料查阅】上述四种物质的相关信息如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下某稀溶液的pH | 7 | 13 | 11 | 9 |
【探究过程】
如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是 ;
在进行操作②时有无色无味得到气体产生,由此又可排除假设物质中的 。
【探究结论】
你认为该溶液中的溶质可能是上述假设物质中的 ,你的判断依据是 。
【探究反思】
(1)若上述探究结论是正确的,操作②产生的气体应是 (写化学式),实验室检验该气体的实验操作及现象是 。
(2)另有同学猜想其中的溶质还可能是Na2SO4,但又没有Na2SO4的上述表列信息。
请你根据以上实验操作的相关现象,判断该溶液中的溶质是否是Na2SO4,并叙述理由: 。