题目内容
把25g石灰石样品放入足量的稀盐酸中,石灰石中的碳酸钙与盐酸恰好完全反应(杂质不反应,也不溶解),生成气体的质量为8.8g.则石灰石中碳酸钙的质量分数为多少?
分析:将二氧化碳的质量代入化学反应方程式来计算碳酸钙的质量,再计算碳酸钙的质量分数;
解答:解:设碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 8.8g
=
解得x=20g
该样品中碳酸钙的质量分数为
×100%=80%
答:样品中碳酸钙的质量分数是80%;
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 8.8g
| 100 |
| x |
| 44 |
| 8.8g |
解得x=20g
该样品中碳酸钙的质量分数为
| 20g |
| 25g |
答:样品中碳酸钙的质量分数是80%;
点评:本题考查学生利用化学反应方程式的计算,利用二氧化碳的质量是解答的关键.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
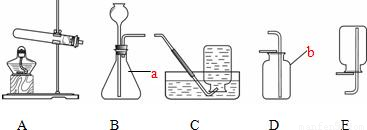
 26、实验室制取气体所需装置如下图所示.
26、实验室制取气体所需装置如下图所示.