题目内容
(2011?翔安区质检)一定质量的纯净物P和32g的物质q在一定条件下按如图所示充分反应,当q反应完全时,可生成44g 物质m和18g 物质n.

下列说法正确的是( )

下列说法正确的是( )
分析:根据质量守恒定律,反应前物质p的质量与参加反应的q物质的质量32g的质量和等于生成物m的质量44g与n的质量18g质量和,由此可计算参加反应的物质p的质量;
由物质q、m、n的分子微观图可知物质q为氧气、物质m为二氧化碳、物质n为水,根据反应前后元素种类、质量不变,则44gm物质中的C元素、18gn物质水中的H元素全部来自于物质p,由物质p中C、H元素的质量和与参加反应物质p的质量关系,可判断物质p的组成,并由二氧化碳、水的质量计算出物质p中组成元素的质量比,进而确定该化学式.据此分析解答即可.
由物质q、m、n的分子微观图可知物质q为氧气、物质m为二氧化碳、物质n为水,根据反应前后元素种类、质量不变,则44gm物质中的C元素、18gn物质水中的H元素全部来自于物质p,由物质p中C、H元素的质量和与参加反应物质p的质量关系,可判断物质p的组成,并由二氧化碳、水的质量计算出物质p中组成元素的质量比,进而确定该化学式.据此分析解答即可.
解答:解:根据质量守恒定律,反应前物质p的质量与参加反应的q物质的质量32g的质量和等于生成物m的质量44g与n的质量18g质量和,由此可计算参加反应的物质p的质量为:44g+18g-32g=30g;
由物质q、m、n的分子微观图可知物质q为氧气、物质m为二氧化碳、物质n为水,根据反应前后元素种类、质量不变,则44gm物质中的C元素、18gn物质水中的H元素全部来自于物质p,则物质m中C元素的质量=44g×
×100%=12g;物质n中H元素的质量=18g×
×100%=2g;其中C、H元素质量和=12g+2g=14g不等于参加反应的p物质的质量,说明物质p中含有C、H、O三种元素,且C、H、O三种元素的质量比=12g:2g:(30g-14g)=6:1:8;则碳氢氧原子个数比是
:
:
=1:2:1,则该气体的最简结构式是CH2O.因此:
A、该反应是两种物质生成两种物质的反应,不属于化合反应,故A错误;
B、经过计算p中含有氧元素,故B错误;
C、p是化合物,故C正确;
D、根据质量守恒定律,参加反应的p的质量是30g,故D错误;
故选项为:C.
由物质q、m、n的分子微观图可知物质q为氧气、物质m为二氧化碳、物质n为水,根据反应前后元素种类、质量不变,则44gm物质中的C元素、18gn物质水中的H元素全部来自于物质p,则物质m中C元素的质量=44g×
| 12 |
| 44 |
| 2 |
| 18 |
| 6 |
| 12 |
| 1 |
| 1 |
| 8 |
| 16 |
A、该反应是两种物质生成两种物质的反应,不属于化合反应,故A错误;
B、经过计算p中含有氧元素,故B错误;
C、p是化合物,故C正确;
D、根据质量守恒定律,参加反应的p的质量是30g,故D错误;
故选项为:C.
点评:此题是微观结构示意图的考查,解题时对原子结构示意图表示的意义的了解,以及根据物质的化学式结合质量守恒定律计算:一定质量的化合物中某种组成元素的质量=化合物的质量×化合物中该元素的质量分数,原子个数比等于各元素的质量除以相对原子质量的比是解题的关键所在.

练习册系列答案
相关题目
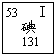 (2011?翔安区质检)碘-131是人工合成的一种放射性同位素,它在元素周期表的信息如图所示,下列关于碘-131的说法不正确的是( )
(2011?翔安区质检)碘-131是人工合成的一种放射性同位素,它在元素周期表的信息如图所示,下列关于碘-131的说法不正确的是( )