题目内容
(2011?翔安区质检)二氧化氮气体 (化学式:NO2) 是一种大气污染物,除去NO2气体常用的方法是用氢氧化钠溶液吸收.
其反应原理为:2NO2+2NaOH=NaNO2+NaNO3+H2O.
(1)请回答:该反应中,N元素化合价最高的含氮化合物是
(2)请计算:要完全吸收9.2g的NO2气体,理论上至少需要10%的NaOH溶液的质量是多少?
其反应原理为:2NO2+2NaOH=NaNO2+NaNO3+H2O.
(1)请回答:该反应中,N元素化合价最高的含氮化合物是
NaNO3
NaNO3
(填化学式)(2)请计算:要完全吸收9.2g的NO2气体,理论上至少需要10%的NaOH溶液的质量是多少?
分析:(1)根据化合物中各元素的化合价代数和为零计算各物质中氮元素的化合价即可;
(2)根据二氧化碳的质量利用方程式直接计算即可;
(2)根据二氧化碳的质量利用方程式直接计算即可;
解答:解:(1)由于化合物中各元素的化合价代数和为零,氧的化合价一般是-2价、钠的化合价是+1,所以NO2、NaNO2、NaNO3中氮元素的化合价分别是:+4、+3、+5,所以N元素化合价最高的含氮化合物是NaNO3;
(2)设至少需要10%的NaOH溶液的质量是x
2NO2+2NaOH=NaNO2+NaNO3+H2O
92 80
9.2g x×10%
=
x=80g
故答案为:(1)NaNO3;(2)理论上至少需要10%的NaOH溶液的质量是80g;
(2)设至少需要10%的NaOH溶液的质量是x
2NO2+2NaOH=NaNO2+NaNO3+H2O
92 80
9.2g x×10%
| 92 |
| 9.2g |
| 80 |
| x×10% |
x=80g
故答案为:(1)NaNO3;(2)理论上至少需要10%的NaOH溶液的质量是80g;
点评:此题是对化合价和方程式计算的考查题,解题的关键是掌握化合价原则以及化学方程式的基本计算;

练习册系列答案
相关题目
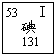 (2011?翔安区质检)碘-131是人工合成的一种放射性同位素,它在元素周期表的信息如图所示,下列关于碘-131的说法不正确的是( )
(2011?翔安区质检)碘-131是人工合成的一种放射性同位素,它在元素周期表的信息如图所示,下列关于碘-131的说法不正确的是( )