题目内容
【题目】下列装置常用语实验室制取气体。请回答下列问题:
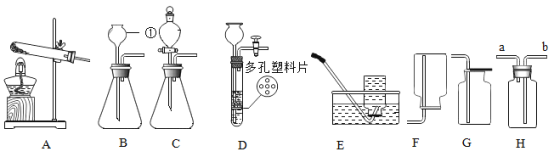
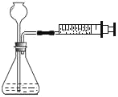
(1)仪器①的名称为_____
(2)实验室利用过氧化氢溶液和二氧化锰制取氧气,若要较好地控制氧气的生成速率且收集较干燥的氧气,应选用装置_____ (填字母,下同),该反应的化学方程式为_____。
(3)实验室若用装置D制取二氧化碳,其优点是_____,若用装置H收集二氧化碳,气体应从_____端进入(填“a”或“b”)。
(4)常温下氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水。实验室常用氯化铵固体与碱石灰固体共热制取氨气,发生装置应选择_____,理由是_____,收集装置应选择_____。
【答案】长颈漏斗 CG或CH 2H2O2![]() 2H2O+O2↑ 可控制反应的发生与停止 b A 反应物都是固体,且反应条件需要加热 F或H
2H2O+O2↑ 可控制反应的发生与停止 b A 反应物都是固体,且反应条件需要加热 F或H
【解析】
(1)仪器①的名称为:长颈漏斗;
(2)实验室利用过氧化氢溶液和二氧化锰制取氧气,若要较好地控制氧气的生成速率,应选用带分液漏斗的固液发生装置C,收集较干燥的氧气,选择项上排空气法收集,选择装置:G或H;故组合装置选:CG或CH;该反应的化学方程式为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(3)实验室若用装置D制取二氧化碳,其优点是:可控制反应的发生与停止;若用装置万能瓶H收集二氧化碳,二氧化碳的密度比空气大,气体“长管进、短管出”应从b端进入;
(4)实验室常用氯化铵固体与碱石灰固体共热制取氨气,选择固体加热装置:A,理由是:反应物都是固体,且反应条件需要加热;常温下氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水。用向下排空气法收集,选择收集装置为:F或H,用H收集时,气体应该选择从a端进气。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】为分析由氧化铜和铜组成的混合物中氧化铜的质量分数,现取3份该混合物各20 g,分别缓慢加入到50 g、100 g、150 g某稀硫酸中,测得三组实验数据如表:
组别 | 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 |
稀硫酸的质量/g | 50 | 100 | 150 |
剩余固体的质量/g | 10.0 | 4.0 | 4.0 |
根据实验及有关数据进行分析与计算:
(1)第Ⅰ组实验中反应物_____________(填“氧化铜”“稀硫酸”或“氧化铜与稀硫酸”)反应完。
(2)20 g样品中含氧化铜的质量为____________g。
(3)根据第Ⅰ组数据计算所用的稀硫酸溶质的质量分数____________(写出计算过程)。
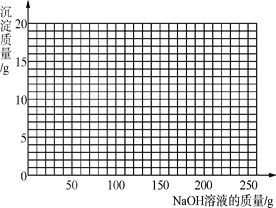
(4)将第Ⅱ组混合物过滤,在滤液中滴加10%的NaOH溶液,画出在该混合溶液中加入10% NaOH溶液的质量与生成沉淀质量变化关系的曲线图___________。